Часть И. ОБЩАЯ
ХИМИЯ
Раздел 5. РОЗЧИНИ.ТЕОРІЯ
ЭЛЕКТРОЛИТИЧЕСКОЙ ДИССОЦИАЦИИ
§
5.14. Решения типовых задач Массовая доля растворенного вещества
Задача 1. Нужно приготовить раствор массой
320 г с массовой долей хлорида калия 3%. Рассчитайте массу КСl и массу воды, которые необходимы для
приготовление раствора.
Решения. Вычисляем массу хлорида
калия, необходимого для приготовления раствора:

где
m - масса
раствора; w (КСl) - массовая доля хлорида
калия.

Вычисляем массу воды, необходимой для
приготовление раствора:
m (Н2О) = m- m(КСl); m(Н2O) = 320-9,6 = 310,4 (г).
Задача 2. Нитрат калия массой 10 г растворили
в воде объемом 150 мл. Плотность воды равна 1 г /мл. Рассчитайте массовую долю
соли в растворе.
Решения. Массу растворителя (воды)
определяем умножением его объема В (Н2О) на плотность р(Н2О):
m(Н2О) = V (Н2O) р(Н2O);m(Н2О) = 150 ∙ 1 =
150 (г).
Вычисляем массу добытого раствора:
m=m (Н2O)+ m (KNO3); m = 150+10=160 (г).
Рассчитываем массовую долю нитрата
калия в растворе:

Задача
3. В воде массой 100
г при температуре 25°С растворяется фосфат калия К3РО4
массой 106 г. Рассчитайте массу фосфата калия, необходимого для приготовления 20 г
раствора К3РО4, насыщенного при температуре 25°С.
Решения. Масса насыщенного при
температуре 25 °С раствора К3РО4, содержащий 100 г воды, равна:
m = m (К3РО4) + m (Н2О); m = 106 + 100 = 206 (г).
Вычисляем массовую долю фосфата
калия в насыщенном при температуре 25 °С в растворе:

Рассчитываем массу фосфата калия,
необходимого для приготовления насыщенного раствора массой 20 г:
m' (К3РО4) = m'w(К3РO4); m' (К3РО4) = 20
∙ 0,515= 10,3
(г).
Задача
4. Кристаллогидрат
нитрата железа(III) Fe(NO3)3 ∙ 9Н2O массой 60,6 г растворили в воде массой
250 г. Определите массовую долю нитрата железа(III) в добытом растворе.
Решения. Масса добытого раствора
составляет:
m =m[Fe(NO3)3
• 9Н2О]+m(Н2O); m = 60,6 + 250 = 310,6 (г).
Определяем
количество вещества кристаллогидрата, растворенного в воде:

С
формулы кристаллогидрата следует:
n [Fe (NO3)3] = n[Fe(NO3)3 • 9Н2О]; n[Fe(NO3)3] = 0,15 (моль).
Находим
массу нитрата железа(III), содержащегося в растворе:
m [Fe (NO3)3] = n
[Fe (NO3)3] М [Fe (NO3)3] ;
m [Fe (NO3)3]
= 0,15 ∙ 242 = 36,3 (г) .
Рассчитываем
массовую долю нитрата железа(III) в растворе:

Задача 5. В лаборатории имеется раствор с массовой
долей гидроксида натрия 25 %, плотность которого равна 1,27 г /мл. Рассчитайте
его объем, который нужно смешать с водой, чтобы добыть 500 мл раствора с массовой
долей NaOH 8
% (плотность 1,09 г /моль).
Решения. При решении
задачи обозначим величины, относящиеся исходному раствору, индексом “1”
(например, m1 - масса исходного раствора);
величины, касающиеся раствора, который нужно приготовить,- индексом “2” (m2
- масса раствора, который нужно приготовить); величины, одинаковые для обоих
растворов, индексами обозначать не будем.
Рассчитываем массу раствора NaOH, который нужно приготовить:
m2
= V2 г2
; m2 = 500 ∙ 1,09 = 545 (г).
Определяем массу чистого NaOH, который будет содержаться в растворе (такая
сама масса гидроксида натрия должна содержаться и в исходном растворе, который будет
разводиться водой):

Вычисляем массу раствора с (NaOH) = 25 %, в котором содержится гидроксид
натрия массой 43,6 г:

Рассчитываем объем исходного раствора
NaOH, который
нужно развести водой:
V1 = m1/p1; V1 = 174,4/1,27 ≈ 137,3 (мл).
Задача 6. К раствору хлорида натрия (объем 120
мл, массовая доля NaCl 16
%, плотность 1,12 г/мл) добавили воду объемом 80 мл (плотность воды 1 г/мл).
Вычислите массовую долю хлорида натрия в добытом растворе.
Розв'язання. вычисляем массу
исходного раствора m1 и массу воды m(Н2O), что добавили:
m1 = V1p1; m1=120 • 1,12 = 134,4 (г);
m(Н2O) = К(Н2O) р (Н2O); m(Н2O) = 80 ∙1 =
80 (г).
Рассчитываем массу добытого раствора:
m2 = m1 + m (Н2О); m2 = 134,4 + 80 = 214,4 (г).
Определяем массу хлорида натрия, который
содержащегося в исходном растворе:
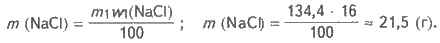
Масса NaCl в растворе после добавления воды также
равна 21,5 г.
Находим массовую долю хлорида
натрия в добытом растворе:

Задача 7. Сероводород объемом 14 мл
растворили в воде массой 500 г (нормальные условия). Вычислите массовую долю
сероводорода в растворе.
Решения. Определяем количество вещества
сероводорода, растворенного в воде:

Масса
растворенного сероводорода составляет: m(H2S) = n(H2S)M[H2S);
m(H2S) = 0,000 625 • 34 = 0,02125 (г).
Находим
массу раствора:
m = m (Н2О) + m
(H2S); m
= 500 + 0,02125 ≈ 500,02 (г). Вычисляем массовую долю сероводорода в
добытом растворе:

Задача 8. В стакан налили 200 мл воды
(плотность 1 г/мл). Определите объем раствора сульфата натрия (массовая доля 12 %,
плотность 1,11 г/мл), который нужно долить в стакан, чтобы получить раствор с
массовой долей Na2SO4 2
%.
Решения. Введем обозначения: m1 - масса исходного раствора сульфата
натрия, в котором w1(Na2SO4) =
12 %. Масса Na2SO4, что
содержится в этом растворе, составляет:
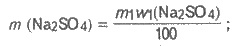

Находим
массу воды в стакане: m(Н2O) = V(Н2O) р (Н2О); m(Н2O)
=
200 -1 = 200 (г).
Вычисляем
массу раствора m2 после добавления в воду исходного раствора сульфата
натрия:
m2 = m1 + m(Н2O); m2 = (m1 + 200) (г).
Следовательно,
в растворе, что имеет массу m2
= (m1 +
200) г, содержится Na2SO4 массой
0,12 m1.
Массовая доля Na2SO4 в этом растворе составляет:

Решив
это уравнение, находим,что m1 = 40 г. Объем раствора, который
нужно добавить в стакан с водой, составляет: V1 = m1/p1; V1 = 40/1,11 = 36 (мл).
Молярная
концентрация
Задача 1. Определите концентрацию молярну
раствора, добытого в Результате растворения сульфата натрия массой 21,3 г в воде
массой 150 г, если плотность добытого раствора равна 1,12 г /мл.
Решения. Определяем массу
добытого раствора:
m = m(Na2SO4) + m(Н2О); m = 21,3 + 150 = 171,3 (г).
Вычисляем объем раствора:
V= m/p; V= 171,3/1,12 =153 (мл) = 0,153 (л).
Количество
вещества растворенного сульфата натрия составляет:

Молярная концентрация раствора с(В) -
это отношение количества растворенного вещества к объему раствора:
с (В) = n(B)/V.
Вычисляем
молярну концентрацию раствора сульфата натрия:
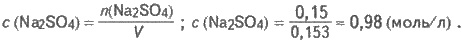
Задача 2. В лаборатории имеется раствор с массовой
долей сульфатной кислоты 5,5 % (плотность 1,035 г/мл). Определите объем этого
раствора, который нужен для приготовления раствора 0,25 М H2SO4 объемом 300 мл.
Решения. Вычисляем количество
вещества серной кислоты (100 %-го раствора), которая нужна для приготовления
раствора 0,25 М H2SO4 объемом 0,3 л: n
(H2SO4) = с (H2SO4) V; n (H2SO4) = 0,25 ∙ 0,3 = 0,075 (моль).
Масса H2SO4
составит: m
(H2SO4) =
n (H2SO4) М
(H2SO4); m (H2SO4) = 0,075 • 98 = 7,35 (г).
Вычисляем массу раствора с массовой
долей сульфатной кислоты 6,5 %, в котором содержится H2SO4 массой 7,35 г:

Определяем объем нужного
раствора:.
V=m/p; V= 133,6/1,035 ≈ 129,1 (мл).
Расчеты
по уравнениям реакций, происходящих в растворах
Задача 1. Какую массу раствора с массовой долей
гидроксида натрия 4 % потребуется для полной нейтрализации соляной кислоты массой
30 г с массовой долей НСl
5 %?
Решения. Составляем уравнение
реакции, что происходит в растворе:
НСl + NaOH = NaCl + Н2О.
Определяем массу и количество вещества
хлороводорода, содержащегося в растворе соляной кислоты:
m(НСl) = mw(НСl); m(НСl) = 30 • 0,05 = 15 (г);
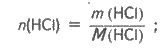

С
уравнения реакции следует:
n(NaOH) = n(НСl); n(NaOH) = 0,0411 (моль).
0,0411 моль - количество вещества
гидроксида натрия, которая требуется для реакции.
Рассчитываем массу
нужного гидроксида натрия:
m (NaOH) = n (NaOH)M (NaOH);
m(NaOH) = 0,0411 ∙ 40 = 1,644 (г).
Определяем необходимую массу m' раствора гидроксида натрия с w(NaOH) = 0,04 (4%):
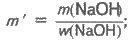
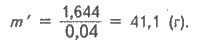
Задача 2. Какой минимальный объем оксида
углерода(IV) необходимо пропустить при нормальных условиях через раствор массой 80 г с массовой
долей гидроксида бария 5 %, чтобы получить гидрокарбонат бария?
Решения. Записываем уравнение
реакции между гидроксидом бария и избытком оксида карбона(ИV):
Ва(ОН)2 + 2СО2
= Ва(НСО3)2.
Определяем
массу гидроксида бария, содержащегося в растворе:
m[Ва(ОН)2] = mw
[Ва(ОН)2];
m[Ва(ОН)2] = 80 0,05 = 4
(г).
Количество вещества гидроксида бария
составляет:

С
уравнения реакции следует:
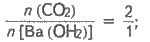
n(CO2) = 2n [Ва(ОН)2];
n(CO2) = 2 • 0,0234 = 0,00468 (моль).
Определяем объем газа
при нормальных условиях:
V(СO2) = n(CO2) • Vm,
V(СO2) = 0,0468 • 22,4 = 1,05 (л).
Задача 3. Определить массовую долю соли, которую добыто
во время смешивания раствора объемом 40 мл с массовой долей азотной кислоты
0,2 и плотностью 1,12 г/мл с долей гидроксида натрия 0,15 и плотностью 1,17 г/мл.
Решения. Введем обозначения:
m1 - масса; V1 - объем; р1 - плотность
раствора азотной кислоты; m2 - масса; V2 - объем; р2 - плотность
раствора гидроокиси натрия; m3
- масса полученного раствора. Записываем уравнение реакции:
HNO3 + NaOH = NaNO3 + Н2О.
Определяем массу и количество вещества
HNO3 в растворе:
m1 = V1p1;
m1 = 40 - 1,12 = 44,8 (г);
m(НNO3) = m1w(HNO3);
m(HNO3) = 44,8 ∙ 0,2 = 8,96 (г);
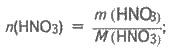

Аналогично находим массу и
количество вещества гидроксида натрия в растворе:
m2 = V2p2;
m2 = 36 1,17 = 42,1 (г);
m(NaOH) = m1w(NaOH);
m(NaOH) = 42,1 • 0,15 = 6,32 (г);
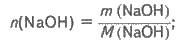
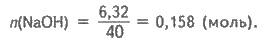
Из уравнения реакции следует, что из
нітратною кислотой количеством вещества 0,142 моль будет реагировать гидроксид натрия
количеством вещества 0,142 моль, следовательно, NaOH взят с избытком.
С
уравнение реакции имеем:
n(NaOH) = n(HNO3); n (NaNO3) = 0,142 (моль).
Определяем
массу соли, образовавшейся:
m(NaNO3) = n(HNO3)
M(NaNO3);
n(NaNO3) =
0,142 85 = 12,1 (г).
Масса
добытого раствора составляет:
m3 = m1 + m2,
m3 = 44,8 + 42,1 = 86,9 (г).
Определяем
массовую долю соли в добытом растворе:


Реакции
обмена в растворах электролитов
Задача 1.
Реакция происходит по уравнению Называемому2+ + 2РО3-4
= Ва3(РO4)2 ↓.
Напишите два различных уравнения в
молекулярной форме, которые соответствуют этим реакциям.
Решения. До ионов в левой части
исходного уравнения допишем ионы с противоположным знаком заряда с таким
коэффициентом, чтобы можно было составить формулы веществ. При этом учитываем, что
исходные вещества должны быть достаточно хорошо растворимыми в воде. Затем те же
ионы с такими же коэффициентами и записываем в правой части уравнения:
Называемому2+ + 2РО3-4
= Ва3(РO4)2 ↓;
6Сl- + 6Н+ = 6Сl- + 6Н+.
Объединяя ионы обоих уравнений в
молекулы, получим уравнение реакции в молекулярной форме:
ЗВаСl2 + 2Н3РO4 = Ва3(РO4)2 и + 6НСl.
Аналогично подбираем и другие ионы,
подходят:
3Ba2+
+ 2РO3-4= Ва3(РO4)2 ↓;
6NO-3
+ 6Na+
= 6NO-3
+ 6Na+.
Получаем второе уравнение в
молекулярной форме:
Называемому(NО3)2 + 2N3РO4 = Ва3(РO4)2 ↓
+ 6NaNO3.
Задача
2. Напишите в
молекулярной и ионной формах уравнения реакций между хлоридом алюминия и нитратом
аргентуму. Приведите пример другой реакции, суть которой выражается таким же
уравнением, что и первой.
Решения. Составляем уравнение
реакции в молекулярной форме:
АlСl3 + ЗАgМЕ3 = gСl↓
+ Аl(NО3)3.
Изобразив вещества, хорошо
диссоциируют, в виде ионов, получим ионное уравнение реакции:

Исключаем из обеих частей равенства
одинаковые ионы, т.е. ионы, не участвующие в реакции (их подчеркнуто).
Записываем сокращенное ионное уравнение реакции:
3Ag+ + ВСl- = 3АgСl↓
или Аg+ + Сl- = АgОl.
С точки зрения теории электролитической
диссоциации суть реакции, что отражает сокращенное ионное уравнение сводится к
взаимодействия ионов аргентуму с хлорид-ионами. Остальные ионов участия в реакции не
берут.
Пример другой реакции, что
выражается тем же уравнением в сокращенной ионной форме:
Аg+ + Сl- = АgСl↓;
NO3- + Н+ = NO3- + Н+.
Уравнение в молекулярной форме:
АglNВ3 + НСl = АgСl↓
+ HNO3.
Водородный
показатель
Задача 1. Принимая, что сульфатная кислота
диссоциирует полностью, определите pH ее
0,012 М раствора.
Решения. Запишем уравнение
полной диссоциации серной кислоты на ионы:
H2SO4 ⇆
2Н+ + SO42-.
Как видим, с 1 моль кислоты
образуется 2 моль Н+. В соответствии с 0,012 моль кислоты образуется
0,024 моль Н+. Концентрация ионов водорода в растворе равна
0,025 моль/л. Отсюда:
pH = -lg[H+]; pH = -lg 0,024 = 1,62.
Задача 2. Определите рн 0,005 М раствора гидроксида натрия.
Решения. В растворе сильный
электролит - гидроксид натрия - полностью диссоциирует на ионы:
NaOH ⇆Na+ + ОН-.
Из 1 моль NaOH образуется 1 моль ОН-, а
0,005 моль NaOH -
0,005 моль ОН-. Следовательно, концентрация ионов ОН- равна
0,005 моль/л.
Зная величину ионного произведения воды
[Н+] [ОН-]
= 10-14, находим концентрацию ионов водорода:

Получаем
pH
= -lg
[Н+]; pH
= -lg[2 ∙ 10-12] = 11,7.
Задача 3. Водородный показатель раствора соляной
кислоты равен 2,1. Определите концентрацию соляной кислоты в растворе.
Решения. Обозначим концентрацию
ионов водорода в растворе х. Тогда - lgх = 2,1 или lgх = -2,1. Преобразуем логарифм таким
образом, чтобы его характеристика была отрицательной, а мантисса - положительной (вычтем
1 и прибавим 1):
рН
= - 2,1 = (-2 -1) + (-0,1 + 1) = - 3 + 0,9 - 3 = lg 10-3 , 0,9 = lg8.
Отсюда
lgx = lg8 + lg 10-3 = lg (8 ∙ 10-3), то есть
[H+] = 8 ∙ 10-3 =
0,008 (моль/л).
В растворе сильная хлоридная кислота
полностью диссоциирует на ионы:
НСl ⇆Н+ + Сl-.
1 моль ионов Н+
образуется из 1 моль НСl,
а 0,008 моль ионов Н+ образуются с 0,008 моль НСl. Следовательно, концентрация соляной
кислоты в растворе составляет 0,008 моль/л.