Часть И. ОБЩАЯ
ХИМИЯ
Раздел 5. РОЗЧИНИ.ТЕОРІЯ
ЭЛЕКТРОЛИТИЧЕСКОЙ ДИССОЦИАЦИИ
§
5.13. Протолітична теория кислот и оснований
Теория электролитической диссоциации
объяснила многочисленные явления и процессы, происходящие в водных растворах
электролитов. Так, например, в различных реакциях нейтрализации
NaOH + НСl = NaCl + Н2O;
КОН + HNO3 = KNO3 + Н2O
одно
и то же значение теплового эффекта (57,3 кДж/моль) объясняется образованием
малодисоційованих молекул воды с Н+ - и ОН- -ионов:
Н+ + ОН- = Н2О.
При
смешивании растворов NaCl и
KNO3
Na+ + С- + К+
+ NO3- =
Na+ +
NO3- +
К+ + Сl-
тепловой
эффект не наблюдается. Это объясняется тем, что химическое взаимодействие между ионами Na+ , Сl-, К+ , NO3- не происходит, как это следует из
ионного уравнения.
Электролитическая диссоциация стала основой
успешного развития теории растворов и изучение процессов, происходящих в них.
В этом заключается ее большое значение в химии. Эта теория не объясняет процессов,
происходят в неводных растворах. Так, например, если хлорид аммония в водном
растворе ведет себя как соль (диссоциирует на ионы NH4 и Сl-), то в жидком аммиаке он обнаруживает
свойства кислоты растворяет металлы с выделением водорода. Как основа ведет
себя азотная кислота, растворенная в жидком фтороводні или в безводной
сульфатной кислоте. Эти факты не согласуются с теорией электролитической
дисоціації. их объясняет протолітична теория кислот и оснований, предложенная в 1923
г. независимо датским ученым И. Бренстедом и английским ученым Т. Лоури.
Согласно этой теории кислотами являются вещества,
молекулы или ионы, которые отщепляют во время протекания данной реакции протоны.
Основаниями являются вещества, молекулы или ионы, которые присоединяют протоны. Как одни, так и
другие получили общее название протолітів.
Реакция отщепления протона
изображается уравнением
Кислота ⇆ Основание + Н+.
Кислота и основа такого процесса
называются сопряженными. Это не кислотно-основная пара. Например, ион Н3О
- кислота, сопряженная основе Н2О, а хлорид-ион Сl- - основа, сопряженная кислоте НСl.
Свободные протоны в растворах самостоятельно
не существуют. Они переходят от кислоты к какой-либо основы. Поэтому в растворе
всегда происходят два процесса:
Кислота1 ⇆
Основа1 + Н+;
Основа2 + Н+ ⇆
Кислота2
i равновесие между ними изображают
уравнением
Кислота1 + Основа2
⇆ Основа1 + Кислота2.
Например, реакцию нейтрализации
ацетатной кислоты аммиаком можно изобразить так:
СН3СООН ⇆
СН3СОО- + Н+;
NH3 + H+ ⇆
NH4+;
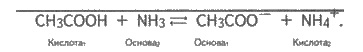
Здесь ацетатная кислота является кислотой
(отдает протоны Н+), аммиак - основой (присоединяет протоны), ионы СН3СОО-
играют роль основы (в этом обратимом процессе они могут принять протоны
и снова превратиться в ацетатну кислоту), а ионы аммония играют роль
кислоты (могут отдать протоны).
Аналогично можно изобразить выявления
основных свойств азотной кислоты, растворенной в жидком фтороводні:
NF
+ HNO3 ⇆ F- + [H2NO3]+.
Кислотаї Основаг Основаї
Кислотаг
Итак, из кислоты и основания всегда
образуются новые сопряженные кислота и основание. Протолітична теория рассматривает
реакцию нейтрализации как переход протона кислоты к основанию. Как видим,
протолітична теория расширила круг кислот и оснований по сравнению с представлениями теории
электролитической диссоциации: ими могут быть также ионы. Одна и та же
вещество в зависимости от того, с чем она реагирует, может быть либо кислотой, либо основанием.
Теория раскрыла относительность понятий о кислоты и основания и показала, что продукты
их взаимодействия следует рассматривать как новые кислоты и основы. Протолітична теория есть
современной и загальнішою теорией кислот и оснований.