КИСЛОТЫ
И ОСНОВЫ
2. Протолітична
равновесие
2.3. Сила кислот и оснований
Слабые кислоты и основания
В
слабых кислот и оснований диссоциация является неполной. Вследствие этого в растворе есть
недисоційовані молекулы.
Поэтому
показатель pH невозможно рассчитать только по концентрации кислоты или основания.
Дополнительно нужна информация о состоянии протолітичної равновесия:

Поскольку
в этом случае концентрация молекул воды гораздо больше, чем концентрация ионов
(Н3О+) и (ОН-), а с(Н2О)
остается практически неизменной, то ее можно объединить вместе с константой
равновесия процесса диссоциации в новую константу:
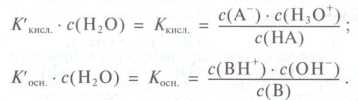
Константа
Ккисл. - константа кислоты, константа Косн. - константа
основы. Для слабых кислот и оснований эти константы очень малы.
Пример.
Етанова (уксусная) кислота - слабая кислота. При 25 °С она диссоциирует по схеме:
НАс + Н2О = Н3О+ + Ас-, константа
кислоты Ккисл. = 1,74 ∙
10-5 моль/л.
В
реакции NH3 + Н2О
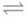 NH4+ + ОН- при 25 °С константа основы Косн.
= 1,78 ∙
10-5 моль/л.
NH4+ + ОН- при 25 °С константа основы Косн.
= 1,78 ∙
10-5 моль/л.
Как
и для водородного показателя, так и для кислот и оснований константа указывается в
виде отрицательного десятичного логарифма:

Пример.
Значение рКкисл. етанової кислоты составляет 4,76. Значение рКосн.
аммиака - 4,75.
Чем
большее значение рКкисл. или значение рКосн., тем слабее
соответствующая кислота или основание.
Между
значением рКкисл. кислоты и значением рКосн. связанной
основы существует такая простая взаимосвязь:
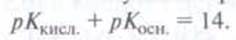
Чем
сильнее кислота, тем слабее связана основа.