КИСЛОТЫ
И ОСНОВЫ
2. Протолітична
равновесие
2.3. Сила кислот и оснований
Силу
кислоты или основания, Бренстедом, определяют способностью к протолізу, что
зависит от того, как сильно выражена готовность вещества отдавать или
принимать протоны. Реагент определяет, какую функцию - кислоты или основания - выполняет
вещество в реакции. В этом случае важным реагентом является вода, поскольку она
выполняет роль основания или кислоты:
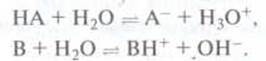
Сильные
кислоты и основания
Для
сильных кислот (НА) или оснований (В) равновесие практически полностью смещено в сторону
образование продуктов реакции.
Внимание:
при растворении гидроксидов в воде протоліз не происходит, поскольку гидроксид-ионы
уже содержатся в твердом гидроксиде.
Водородный
показатель сильных кислот и оснований вследствие полной диссоциации определяется только
соответствующей их концентрации в водных растворах.
Пример.
1 литр 0,5-молярной соляной кислоты содержит также 0,5 моль ионов Н30+.
Водородный показатель раствора составляет, соответственно,
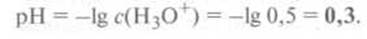
1
литр 0,5-молярного раствора едкого натра также содержит 0,5 моль ионов ОН-.
Луг
имеет показатель pH =14 - 0,3 = 13,7.