КИСЛОТЫ
И ОСНОВЫ
2. Протолітична
равновесие
2.2. Водородный показатель
В
водных растворах электролитов (кислот, оснований) ионное произведение воды остается
практически неизменным, пока их концентрация не станет очень большим.
Следовательно,
если концентрация с(Н3О+) в растворе больше, чем в чистой
воде, то с(ОН-) должна быть меньше, и наоборот.
Пример.
Равновесие НСl
+ Н2O
 Н3O+ + Сl-
практически полностью смещено в сторону продуктов реакции. Потому 0,1 - молярный раствор
соляной кислоты имеет концентрацию с(Н3О+) = 0,1 моль/л = 10-1 моль/л. Следовательно,
концентрация гидроксид-ионов будет равна:
Н3O+ + Сl-
практически полностью смещено в сторону продуктов реакции. Потому 0,1 - молярный раствор
соляной кислоты имеет концентрацию с(Н3О+) = 0,1 моль/л = 10-1 моль/л. Следовательно,
концентрация гидроксид-ионов будет равна:
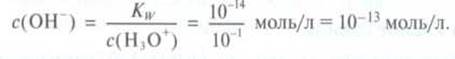
Запомните: в кислых растворах концентрация ионов гідроксонію
больше, чем концентрация гидроксид-ионов. В щелочных растворах концентрация
гидроксид-ионов больше, чем концентрация ионов гідроксонію.
Чтобы
определить, является ли раствор кислым или щелочным, достаточно указать с(Н3О+)
или с(ОН-). Водородный показатель определяет значение с(Н3О+)
в виде шкалы положительных числовых значений от 0 до 14. В то же время:
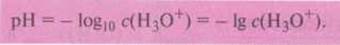
Пример.
Хлоридная кислота, в которой С(Н3О+) = 10-1
моль/л, имеет водородный показатель pH = 1.
С
значений водородного показателя следует:
|
Водородный показатель
|
с(Н3О+)
моль/л
|
с(ОН-) в моль/л
|
Раствор
|
|
0-7
|
100 - 10-7
|
10-14 - 10-7
|
кислый
|
|
7
|
10-7
|
10-7
|
нейтральный
|
|
7-14
|
10-7 - 10-14
|
10-7 - 100
|
лужный
|
Запомните:
чем кислее раствор, тем меньше значение водородного показателя, чем более щелочным является
раствор, тем выше показатель pH.
Кроме
показателя pH, для характеристики с(ОН-) применяют показатель
рОН:
