КИСЛОТЫ
И ОСНОВЫ
1. Определения кислот и оснований
Кислотами
обычно считают вещества, водные растворы которых имеют такие свойства:
♦ кислый вкус;
♦ растворяют неблагородные металлы, выделяя
водород;
♦ разлагают карбонаты (например, известняк) с
выделением карбон диоксида;
♦ изменяют окраску индикаторов.
К
основ относятся вещества, водные растворы которых (щелочи) имеют такие свойства:
♦ мыльные на ощупь;
♦ изменяют окраску индикаторов;
♦ нейтрализуют кислоты.
Исходя
из перечисленных свойств, существуют различные определения кислот и щелочей.
1.1. Развитие понятий «кислоты» и «основания»
Некоторые
оксиды неметаллов реагируют с водой, образуя вещества, водные растворы которых
кислые. Отсюда в 1775 г. было дано первое определение кислот.
Кислородосодержащие
кислоты образуются в результате реакции оксидов неметаллов с водой (Антуан Лавуазье).
Пример.
Сульфур диоксид и фосфор(V)
оксид реагируют с водой, образуя сульфітну и фосфатную кислоты:
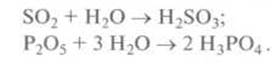
С
другой стороны, некоторые оксиды металлов, вступая в реакцию с водой, образуют
гидроксиды, водные растворы которых имеют щелочные свойства.
Пример.
Кальций оксид реагирует с водой, образуя кальций гидроксид. Водный раствор
(известковая вода) является щелочью:
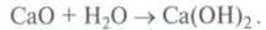
Более
общее определение кислот, поданное в 1838 г., рассматривает как кислородосодержащие, так
и безоксигенові кислоты.
Кислоты
- это вещества, содержащие Водород, который может замещаться металлом (Юстут фон Либих).
Пример.
Хлоридная кислота растворяет магний с выделением водорода:

Следующее
определение кислоты, поданное в 1887 г., исходит из того факта, что водные растворы
кислот и щелочей содержат ионы Водорода или гидроксид-ионы.
Кислоты
- вещества, которые при растворении в воде отщепляют ионы Водорода (протоны).
Основания - вещества, которые при растворении в воде отщепляют гидроксид-ионы (Сванте Ареніус).
Пример.
Газообразный водород хлорид при растворении в воде отщеплять протоны, а твердый
натрий гидроксид при растворении в воде отщепляет гидроксид-ионы.
Запомните:
распад веществ на ионы называют диссоциацией.