КИСЛОТЫ
И ОСНОВЫ
1. Определения кислот и оснований
1.2.
Теория Бренстеда
Много
веществ образуют кислые или щелочные растворы, но не соответствуют приведенным
определением кислот и щелочей.
Пример.
Раствор аммоний хлорида имеет кислую реакцию, а раствор натрий ацетата - щелочную.
В
связи с этим Иоганн Бренстед и Томас Лоури
сформулировали в 1923 г. новое определение кислот и оснований.
Кислота
может отдавать протоны, а основа принимать протоны. Кислота является донором протонов,
а основание - акцептор протонов.
Пример.
При диссоциации гидроген хлорида в растворе образуется хлоридная кислота.
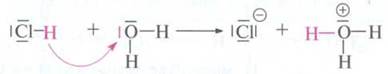
Молекула
гидроген хлорида отщепляет протон, то есть является кислотой, а молекула воды принимает
протон и является, таким образом, основой. За счет присоединения протона к молекуле
воды образуется ион гідроксонію (оксонію).
Пример.
Аммиак реагирует с водой, образуя щелочной раствор.
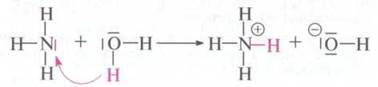
Молекула
аммиака принимает протон, выступая в роли основы. Молекула воды отдает протон,
поэтому в данном случае является кислотой. За счет присоединения протона к молекуле
аммиака образуется ион аммония.
Оба
примеры показывают, что молекулы воды могут выступать как в роли основ, так и
кислот.
Которая
частица в кислотно-основной реакции является кислотой или основанием, зависит от того,
который из двух реагентов имеет большую способность отдавать протоны или принимать их.
Запомните:
понятия «кислота» и «основание» характеризуют функцию, а не вещество.
На
отличие от предыдущих определений, согласно определению Бренстеда, реакция
образование кислоты и основания может происходить и без участия воды.
Пример.
Хлоридная кислота реагирует с амоніаком, образуя аммоний хлорид.
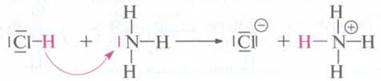
Молекула
гидроген хлорида отдает протон, выступлениями таким образом кислотой, а молекула
аммиака принимает протон, поэтому является основой.
В
реакции с соответствующей пары кислоты и основания всегда возникает новая пара: кислота
и основа. Обе стороны отражают химическое равновесие.
Обобщение
теории Бренстеда:
♦ реакция образования кислоты и основания есть
переносом протонов. Переход протонов от кислоты к основанию называют протеолізом;
♦ частицы, связанные между собой переходом
протона, называют сопряженными парами кислота-основа.
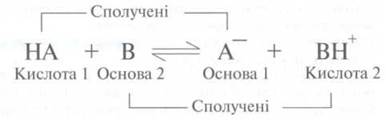
Процесс
протолізу, в котором сильнее кислота переносит протон на более сильную основу, ведет
к протолітичної равновесия.
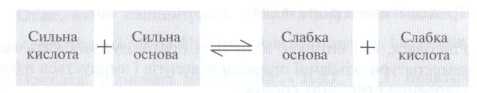
Запомните:
протолітична равновесие всегда смещается в сторону образования более слабой кислоты или
основы.
Пример.
При образовании соляной кислоты молекула гидроген хлорида является более сильной кислотой
относительно иона гідроксонію, а молекула воды является более сильной основой относительно
гидроген хлорида. Поэтому равновесие смещено вправо.