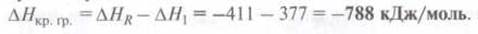ЭНЕРГЕТИКА ХИМИЧЕСКИХ РЕАКЦИЙ
2.
Изменение энергии при кристаллизации и растворении
В
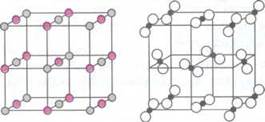
твердом агрегатном состоянии вещества образуют, как правило, решетку, в которой
частицы упорядоченно соединенные между собой. Взаимодействие между ионами обусловлена
кулонівськими силами, между молекулами - вандерваальсовими силами.
2.1. Внутренняя энергия кристаллических веществ
Образование
кристаллической решетки из составляющих частиц - это экзотермический процесс.
Энергию,
которая выделяется при образовании кристаллической решетки из составных частей,
называют энергией кристаллической решетки.
Энергию
кристаллической решетки вещества непосредственно определить невозможно. Так называемый цикл
Борна-Габера однако позволяет определить энергию кристаллической решетки косвенным
путем, используя закон Гесса.
Пример.
Энергия кристаллической решетки натрия хлорида (поваренная соль) составляет -788
кДж/моль. Таким образом, чтобы расщепить 1 моль поваренной соли на ионы Натрия и ионы
Хлора, нужно затратить энергию в 788 кДж.
Это
значение энергии можно рассчитать из тепловых эффектов нескольких промежуточных
реакций, которые можно осуществить экспериментальным путем:
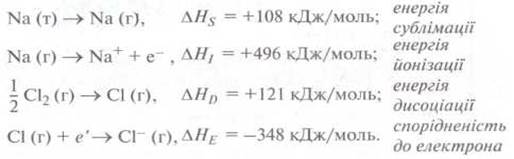
Суммарная
изменение энергии реакции превращения 1 моль твердого натрия ионы Натрия и 1/2
моль газообразного хлора в ионы Хлора рассчитываем из суммы энергий отдельных
стадий:
∆H1 = + 108 + 496 +121 - 348 = 377
кДж/моль.
Эти
реакции дают в целом эндотермический эффект.
Однако
образование 1 моль твердой поваренной соли с 1 моль твердого натрия и 1/2 моль газообразного
хлора проходит как экзотермический процесс с энтальпией реакции ∆HR = -411 кДж/моль.
Энергия
кристаллической Решетки - это та энергия, которая выделяется при образовании 1 моль
твердой поваренной соли из газообразных ионов Натрия и Хлора.
Энергию
кристаллической Решетки получаем как разность энергии реакции образования 1 моль
твердой соли с 1 моль твердого натрия и 1/2 моль газообразного хлора и выше
рассчитанной суммы энергий: