ЭНЕРГЕТИКА ХИМИЧЕСКИХ РЕАКЦИЙ
1. Превращения энергии в химических реакциях
Практически
во всех химических реакциях происходит взаимное превращение различных видов
энергии. Чаще всего энергия выделяется или поглощается в виде теплоты.
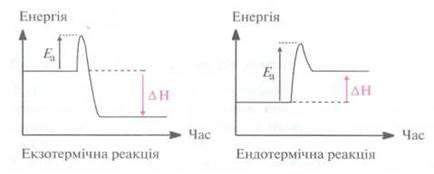
Если в ходе реакции энергия выделяется, то такую реакцию называют
экзотермической, если энергия поглощается, то такую реакцию называют
эндотермическим реакцией.
Пример.
Магний реагирует с кислородом, образуя магний оксид. При этом энергия выделяется в
виде теплоты и света:
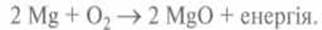
Азот
реагирует с кислородом, образуя азот(II) оксид, лишь поглощая энергию:

Большинство
реакций происходит только после активации реагентов. Нужная для этого энергия
активации Еа обычно
используется в виде теплоты.
1.1. Энтальпия образования соединений
Энергию,
которая выделяется или поглощается при образовании 1 моль соединения из простых веществ,
называют энтальпией образования ∆Нf. Энтальпия образования зависит от
температуры и давления.
Если
в ходе реакции энергия выделяется, то ∆Нf
0, а если поглощается, то ∆Нf > 0.
Пример.
При температуре Т = 298,16 К (= 25 °С) и давлении р = 101,3 кПа энтальпия
образование магний оксида составляет ∆Н0f,298
= -601 кДж/моль, т.е. при образовании 1 моль магний оксида из простых веществ при
этом выделяется 601 кДж.
Энтальпия
образование нитроген(II) оксида при тех же условиях составляет ∆Н0f,298
= + 90 кДж/моль, т.е. для образования 1 моль нитроген(II) оксида из простых
веществ поглощается 90 кДж.
Температура
Т = 298,16 К и давлении р = 101,3 кПа являются стандартными условиями, соответствующую энтальпию
образование называют стандартной энтальпией образования ∆Н0f,298.
Внимание:
стандартные условия не следует путать с нормальными условиями: ТН = 273,16
К (= 0 °С) и рр = 101,3 кПа.