Часть III. ОРГАНИЧЕСКАЯ ХИМИЯ
Раздел 15. ОСНОВНЫЕ ПОЛОЖЕНИЯ ОРГАНИЧЕСКОЙ
ХИМИИ
§
15.2. Особенности органических соединений
На
отличие от неорганических веществ органические соединения имеют ряд характерных
особенностей. Прежде всего атомы углерода способны соединяться друг с другом,
образуя цепи и кольца, что не так типично для неорганических соединений. Это одна из
причин разнообразия органических соединений.
В органических молекулах связь
атомов ковалентная. Поэтому органические вещества обычно являются неэлектролитами.
Если ионные (неорганические) соединения
легко диссоциируют в воде на ионы и реакции между ними происходят достаточно быстро,
то органические вещества, содержащие простые (одинарные) С-С и С-Н - связи,
взаимодействуют между собой очень трудно или совсем не взаимодействуют.
При нагревании в пределах 400-600 °С
органические соединения полностью разлагаются и обугливаются, а при наличии кислорода
сгорают. Это объясняется сравнительно небольшой прочностью связи между атомами
карбона (355,6 кДж/моль).
Важной особенностью органических
соединений является и то, что среди них широко распространено явление изомерии (см. § 15.3).
Особенности атома углерода
объясняются его строением: он имеет четыре валентных электрона. Атомы карбона
образуют с другими атомами, а также друг с другом общие электронные пары. При
этом на внешнем уровне каждого атома углерода будет восемь электронов (октет),
четыре из которых одновременно принадлежат другим атомам.
В органической химии конечно
пользуются структурными формулами, поскольку атомы имеют пространственное размещение
в молекуле. Структурные формулы - это язык органической химии.
В структурных формулах ковалентная
связь обозначается чертой (см. § 3.10). Как и в структурных формулах
неорганических веществ, каждая черточка означает общую электронную пару, которая связывает
атомы в молекуле. Используются также эмпирические и электронные формулы. Такие
формулы показано в § 3.8 для молекул воды, аммиака и метана. Напишем
соответствующие формулы для этилена и ацетилена:
Эмпирические формулы:
С2Н4 С2Н2
Электронные
формулы: 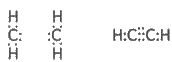
Структурные
формулы: 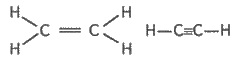
Как отмечалось в § 3.10, в
органической химии вместо понятия степени окисления применяют понятие
валентности. Валентность атома углерода в возбужденном состоянии всегда равна
четырем: он образует четыре ковалентных связи.