КЛАССЫ
ОРГАНИЧЕСКИХ ВЕЩЕСТВ
9. Протеины (белки)
Основными
строительными блоками белков являются аминокислоты, связанные между собой в виде
цепи. В зависимости от размера полученного полимера различают пептиды (2-9 остатков
аминокислот), полипептиды (10-100 остатков аминокислот) и протеины (более 100
остатков аминокислот).
9.1. Аминокислоты
Аминокислоты
кроме функциональной карбоксильной группы включают аминогруппу (-NH2). В природных аминокислотах аминогруппа
всегда связана с атомом Углерода, который находится рядом с карбоксильною
группой.
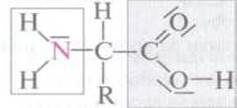
Запомните:
природные аминокислоты называют 2-аминокислотами (α-аминокислоты).
Аминокислоты,
за исключением глицина (R = Н), являются оптически активными соединениями.
Все α-аминокислоты,
которые встречаются в протеинах, имеют L-конфигурацию.
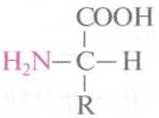
Свойства аминокислот
Аминокислоты
- твердые вещества, хорошо растворимые в воде, имеют высокие температуры плавления,
находящихся в пределах 175-300 °С. Молекулы этих кислот должны, таким образом,
воздерживаться сильными электростатическими силами, которые возникают в ионных решетке.
Внутри
молекулы аминокислоты происходит внутренне-молекулярный протоліз, при котором
карбоксильная группа отдает один протон, а аминогруппа его получает. Так
образуется амфотерный ион (внутренняя соль).
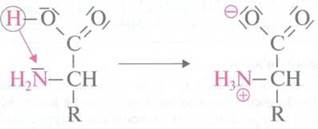
Сильное
взаимное притяжение амфотерных ионов в аминокислотах обеспечивает высокую
стабильность кристаллической решетки. В состав молекул аминокислот входят основная
группа -NH2 и
кислотная группа-СООН, что обуславливает их амфотерные свойства, то есть они
образуют соли как с кислотами, так и с основаниями. Молекулы кислоты в растворе
находятся как амфотерные ионы (внутренняя соль). Каждая аминокислота в ізоелектричній
точке характеризуется водородным показателем.
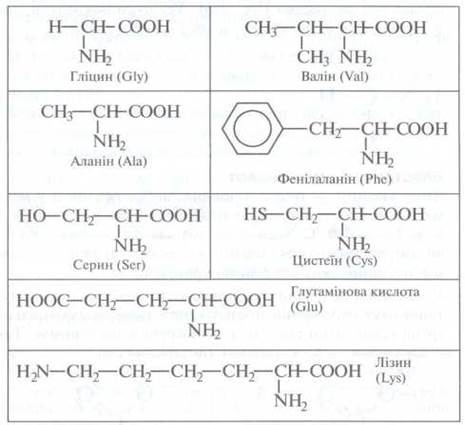
Таблица
некоторых важных аминокислот