Часть II.
НЕОРГАНИЧЕСКАЯ ХИМИЯ
Раздел 10. ПОДГРУППА
АЗОТА
§
10.3. Аммиак
Строение молекулы. Азот образует с
гідрогеном несколько соединений, из которых важнейшим является аммиак. Электронная формула
молекулы аммиака такая:
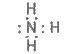
Видно, что из четырех электронных пар
у азота - три общие (связующие) и одна неразделенная (незв'язуюча).
Строение
молекулы NH3 рассмотрено
ранее (см. рис. 3.4). Она имеет форму пирамиды. Химическая связь N-Н полярный: положительный заряд
сосредоточен на атомах водорода, отрицательный - на атоме азота. Вследствие
этого между молекулами аммиака образуется водородная связь,что можно
изобразить так:
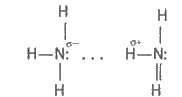
Вследствие водородных связей
аммиак имеет сравнительно высокие температуры плавления и кипения, а также значительную
теплоту испарения, он легко сжижается.
Физические свойства. Аммиак -
бесцветный газ с характерным резким запахом, почти в два раза легче
воздуха. При увеличении давления или охлаждении он легко сжижается в бесцветную
жидкость (температура кипения -33,4°С). Аммиак очень хорошо растворяется в воде (при
20°С в 1 объеме воды растворяется до 700 объемов NH3).
Раствор аммиака в воде называется
аммиачной водой или нашатырным спиртом. Во время кипячения растворенный аммиак
звітрюється из раствора.
Химические свойства. Большая растворимость
аммиака в воде обусловлена образованием водородных связей между их молекулами:
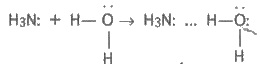
Однако, кроме таких гидратов аммиака,1
частично образуются ионы аммония и гидроксид-ионы:
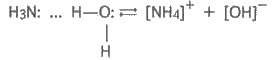
Гидроксид-ионы обусловливают
слабощелочную (их мало) реакцию аммиачной воды. При взаимодействии их с ионами NH+4 вновь образуются молекулы NH3 и Н2О, соединенные водородным
связью, т.е. реакция происходит в обратном направлении. Образование ионов
аммония и гидроксид-ионов в аммиачной воде можно изобразить уравнением:
NH3 + Н2O ⇆
NH3 ∙ Н2О ∙ NH+ + ОН-.
В
аммиачной воде наибольшая часть аммиака содержится в виде молекул NH3, равновесие смещено в сторону образования
аммиака, поэтому она пахнет аммиаком. Несмотря на это, водный раствор аммиака по
установленной традиции обозначают формулой NH4OH 1 и называют гидроксидом аммония, а
щелочную реакцию раствора объясняют диссоциацией молекул NH4OH:
NH4OH
⇆NH+ + ОН-
Поскольку в растворе аммиака в воде
концентрация гидроксид - ионов невелика, гидроксид аммония относится к слабым
основ.
Следовательно, в реакции взаимодействия аммиака с
водой к молекуле аммиака присоединяется протон из воды, вследствие чего образуется
катион аммония NH+4 и
гидроксид-ион ОН . В катіоні аммония четыре ковалентных связи, один из них
образованная по донорно-акцепторным механизмом (см. § 3.1).
Важным химическим свойством аммиака
является его взаимодействие с кислотами с образованием солей аммония. В этом случае к
молекулы аммиака присоединяется ион водорода кислоты, образуя ион аммония,
входит в состав соли:
NH3 = НСl + NH4Cl; .
NH3 + Н3РО4 = NH4H2PO4.
Из приведенных примеров следует, что
для аммиака характерна реакция присоединения протона.
Аммиак сгорает в кислороде и в воздухе
(предварительно подогретом) с образованием азота и воды:
4NH3 + 3О2 = 2N2 + 6Н2О.
При наличии катализатора
(например, платины, оксида хрома(III)) реакция происходит с образованием
оксида азота(II) и воды:
4NH3 + 5O2 = 4NO + 6Н2О.
Эта
реакция называется каталитическим окисненням аммиака.
1 Поскольку такого вещества нет, то
вопреки традиции ее можно изображать как гидрат NН3 ∙ Н2О
или просто NН3 (без гидроксид-иона).
Аммиак - сильный восстановитель. При
нагревании он восстанавливает оксид купруму(II), сам окисляется до свободного азота:
+2
-3
0 0
ВСuО + 2NH3 = ВСu + N2 + ЗН2О;
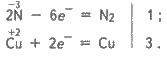
С помощью этой реакции можно
добыть азот в лабораторных условиях.
Добывания и применения. В
лабораторных условиях аммиак обычно получают слабым нагреванием смеси хлорида
аммония с гашеной известью:
2NH4Cl+ Са (ОН)2 = Саси2
+ 2NH3 ↑ + 2Н2О.
Эта реакция основывается на смещении равновесия
взаимодействия аммиака с водой при добавлении гидроксид-ионов:
NH+ + ОН- ⇆
NH3 ↑ + Н2O.
Основным способом добывания аммиака в
промышленности является его синтез из азота и водорода. Реакция экзотермическая и оборотная:
N2 + ЗН2 ⇆
2NH3, ∆
Н° = -92,4 кДж.
Она происходит только за
наличии катализатора - губчатого железа с добавками активаторов - оксидов
алюминия, калия, кальция, кремния (иногда и магния). Исходные продукты добывают:
азот - из жидкого воздуха, водород - конверсионным способом или с воды (см. §
8.2).
Большие количества аммиака тратятся
для добывания азотной (азотистой) кислоты, азотсодержащих солей, мочевины, соды
по аммиачным методом. На легком прореживании и последующем испарении с
поглощением теплоты основывается "его применения в холодильном деле.
Жидкий аммиак и его водные растворы
применяют как жидкие удобрения.
1 Гидраты - продукты присоединения воды
к веществам.