Часть II.
НЕОРГАНИЧЕСКАЯ ХИМИЯ
Раздел 10. ПОДГРУППА
АЗОТА
§
10.2. Азот. Сигма - и пи-связи
Распространение в природе. Азот в природе
случается преимущественно в свободном состоянии. В воздухе объемная доля его составляет
78,09 %, а массовая доля - 75,6 %. Соединения азота в небольших количествах есть в
грунте. Азот входит в состав белковых веществ и многих природных
органических соединений. Общее содержание азота в земной коре составляет 0,01 %.
Добывания. В технике азот добывают
из жидкого воздуха. Как известно, воздух - это смесь газов, преимущественно азота и
кислорода. Сухой воздух у поверхности Земли содержит (в объемных долях): азота
78,09 %, кислорода 20,95 %, благородных газов 0,93 %, оксида карбона (IV) 0,03 %, а
также случайные примеси - пыль, микроорганизмы, сероводород, оксид серы (IV)
и др. Для добывания азота воздух переводят в жидкое состояние, затем
испарением отделяют азот от менее леткого кислорода (т. кип. азота -
195,8, кислорода - 183 °С). Добытый таким образом азот содержит примеси благородных
газов (в основном аргон). Чистый азот можно получить в лабораторных условиях,
разлагая при нагревании нитрит аммония:
NH4NO2 = N2 ↑ +
2Н2О.
Сигма - и пи-связи. Для объяснения
физических и химических свойств простого вещества азота необходимо подробнее
рассмотреть строение его молекулы. Как следует из электронного строения внешнего
уровня атома азота (см. § 2.7), его химические связи осуществляются тремя
неспареними р-электронами каждого атома; г-орбитали имеют форму гантели и
направленные вдоль оси пространственных координат. Это рх, Ру-
и pz-
орбітапі. Образование химических связей является результатом перекрывания орбиталей
атомов (§ 3.1). Образование тройной связи в молекуле азота можно представить, как
показано на рис. 10.1 (в молекуле N2 химическая связь осуществляется за счет трех
совместных пар р-электронов, орбитали которых направлены по осям х, y, z).
Ковалентная связь,
образуется при перекрывании орбиталей вдоль линии, связывающей центры атомов,
которые соединяются, называется о (сигма)-связью.
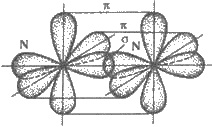
Рис. 10.1. σ - и п-Связи в молекуле азота
Все одинарные связи является a-зв'язками. гу- и pz-Орбитали, которые остались,
перекрываются по обе стороны от линии, соединяющей центры атомов (рис. 10.2).
Ковалентная связь возникает
при перекрывании орбиталей по обе стороны от линии, соединяющей центры атомов,
которые зв обязуются, называется п (пи)-связью.
Следовательно, в молекуле азота есть один
σ - связь и две п-связи, вместе три связки, что можно изобразить так:
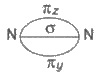
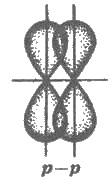
Рис. 10.2. Схема образования п-связи
Физические
свойства. Азот - газ без цвета, запаха и вкуса, легче
воздуха.
Растворяется в воде хуже, чем кислород: при 20 °С в 1 л воды растворяется 15,4
мл азота (кислорода - 31 мл). Поэтому в воздухе, растворенном в воде, содержание кислорода
в отношении азота больше, чем в атмосферном. Малая растворимость азота в воде, а
также его очень низкая температура кипения объясняются довольно слабыми
межмолекулярными взаимодействиями как между молекулами азота и воды, так и между
молекулами азота.
Природный азот состоит из двух
стабильных изотопов с массовыми числами 14 (99,64 %) и 15 (0,36 %).
Химические свойства. Молекула азота состоит
из двух атомов. Длина связи между ними очень мала - 0,109 нм. Тройная связь
и его малая длина делают молекулу очень прочной (энергия связи 946
кДж/моль). Этим объясняется малая реакционная способность азота при обычной
температуре (сравнить с O2 и Сl2).
При комнатной температуре азот
непосредственно соединяется только с литием:
6Li
+ N2 = 2Li3N.
Нитрид лития
С другими металлами он реагирует только
при высокой температуре, образуя нитриды. Например:
Оса
+ N2 = Ca3N2;
2Аl + N2 = 2AlN.
Нитрид кальция
Нитрид алюминия
С водородом азот соединяется по
наличии катализатора, при высоких давления и температуры:
N2 + ЗН2 ⇆ 2NH3.
При температуре электрической дуги (3
000-4 000 °С) азот соединяется с кислородом:
N2 + O2 ⇆2NO.
Поскольку на внешнем
энергетическом уровне атома азота находится 5 электронов, азот обнаруживает
степени окисления -3 и +5, а также+4, +3, +2, +1, -1 и-2.
Применение. В больших количествах
азот применяется для извлечения аммиака. Широко используется для создания
инертной среды - наполнения электрических ламп накаливания и свободного
пространства в ртутных термометрах, при перекачке горючих жидкостей. Им азотують
поверхность стальных изделий, т.е. насыщают их поверхность азотом при высокой
температуры. В результате в поверхностном слое образуются нитриды железа, которые
предоставляют стали большей твердости. Такая сталь выдерживает нагревание до 500°С без
потери своей твердости.
Большое значение азот имеет для жизни
растений и животных, поскольку он входит в состав белковых веществ. Соединения
азота применяются в производстве минеральных удобрений, взрывчатых веществ и
во многих других отраслях промышленности.