УГЛЕРОД И ЕГО СОЕДИНЕНИЯ
УГЛЕРОД КАК ПРОСТОЕ ВЕЩЕСТВО
В атоме Углерода на его внешних
четырех АО имеется четыре электрона, поэтому все четыре АО принимают участие в образовании
химических связей. Этим объясняется разнообразие и многочисленность соединений
Карбона. Подавляющее большинство соединений Углерода относится к так называемых органических
веществ. В этом разделе рассматриваются свойства неорганических веществ,
образованных Карбоном, - простых веществ, его оксидов, карбонатной кислоты и
некоторых ее солей.
Карбон образует несколько простых
веществ. Среди них важнейшими являются алмаз и графит. Эти аллотропные модификации
имеют атомные кристаллические решетки, которые отличаются своими структурами. Отсюда и
различие их физических и химических свойств.
В алмазе каждый атом Углерода
соединен с четырьмя другими атомами. В пространстве эти атомы располагаются в
центре и углах тетраэдров, соединенных вершинами. Это - очень симметричная и прочная
решетка. Алмаз - самое твердое вещество на Земле.
В графите каждый атом соединен с
тремя другими, которые лежат в той же плоскости. На образование этих связей
затрачивается по три АО с тремя электронами. Четвертая орбиталь 2р-АО с одним
электроном располагается перпендикулярно к плоскости. Те атомные орбитали, которые
остались из всей сетки, перекрываются между собой, создавая зону молекулярных
орбиталей. Эта зона занята не полностью, а наполовину, что обеспечивает металлическую
электропроводность графита (в отличие от алмаза).
Кроме электропроводности графит
владеет еще тремя важными свойствами.
Во-первых, тугоплавкость. Температура
плавления графита выше 3500 °С - это найтугоплавкіша простое вещество на Земле.
Таблица
Углерод и его соединения
|
Углерод
|
Соединения Карбона
|
|
оксид углерода (IV)
|
карбонатная кислота
|
|
1. Имеет
аллотропные модификации: алмаз, графит, карбин, фуллерен и др.
2. Проявляет
восстановительные свойства:
а) горит
в кислороде:
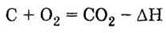
неполное
сгорания:
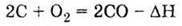
б) взаимодействует
с оксидом углерода (IV):

в) восстанавливает
металлы из их оксидов:
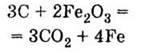
Получение
Неполное
сгорания метана:
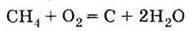
|
1. Газ
без запаха, цвета и вкуса, тяжелее воздуха
2. Кислотный
оксид
3. При
растворении взаимодействует с водой:
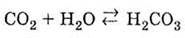
4. Реагирует
с основами:
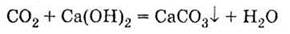
5. Реагирует
с основными оксидами:
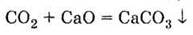
6. Образуется
в реакциях
а) горения
углерода в кислороде:
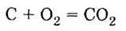 ґ ґ
б) окисления
оксида углерода (II):
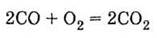
в) сгорания
метана:
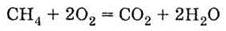
г) взаимодействие
кислот с карбонатами:
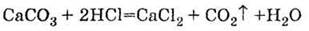
ґ)
термического разложения карбонатов и гидрокарбонатов:
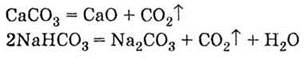
д) окислительных
биохимических процессов дыхания, гниения
|
1. Неустойчивая
молекула. Слабая двохосновна кислота. В водном растворе существует равновесие:
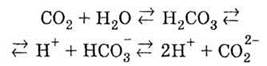
2. Взаимодействует
с растворами щелочей как раствор углекислого газа в воде 3 образованием солей -
кислых (гидрокарбонатов) и средних (карбонатов):
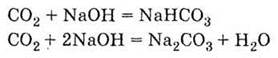
3. Вытесняется
из солей более сильными | кислотами:
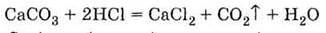
4. Соли
карбонатной кислоты подвергаются гидролизу:
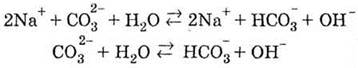
|
Во-вторых, отсутствие на его
поверхности любых продуктов взаимодействия с окружающей средой (на металлах это
оксиды), которые увеличивают электрическое сопротивление.
В-третьих, имеет свойство смазывать
поверхности, которые трутся. В кристалле графита атомы Углерода прочно соединены между
собой в плоских сетках, а связь между сетками слабый: он имеет міжмолекулярну
природу, как и в веществах с молекулярными ґратками, поэтому даже незначительные
механические усилия вызывают смещение сеток относительно друг друга, что и обуславливает
действие графита в качестве смазки.
Энергия связи между атомами Углерода
в простых и сложных веществах, в том числе в алмазе и в граффити, очень большая.
О твердость алмаза уже упоминалось. Прочная связь между атомами и в графитовой
сетке. Так, прочность на разрыв волокна из графита значительно превышает прочность
железа и технической стали.
На основе графита изготавливают так
называемые композиционные материалы, в частности карбопластики, в которых волокна графита
находятся в матрице из эпоксидной смолы. Композиционные
материалы все шире применяются в авиационной и космической технике
(ведь, кроме прочности они легкие; сравните плотность графита, ρ = 2,3 г/см3,
с плотностью «легкого» алюминия ρ = 2,7 г/см3, и, тем более,
железа, ρ = 7,9 г/см3), а также в кораблестроении, где особенно
ценные противокоррозионные свойства.
Углерод химически инертен только при
сравнительно низких температурах, а при высоких - это один из сильнейших
восстановителей. В химии, в основном, углерод применяют для восстановления
металлов, прежде всего железа, из руд; в предыдущем разделе упоминалось его
использование для получения фосфора.