ХИМИЯ НЕМЕТАЛЛИЧЕСКИХ ЭЛЕМЕНТОВ
ФОСФОР И ЕГО СОЕДИНЕНИЯ
Радиус атома Фосфора почти в два
раза больше, чем Азота. Это предопределяет существенные различия в их
свойствах.
Разница в размерах атомов
сказывается уже в строении простых веществ. Молекулы азота, образованные маленькими
атомами, двухатомные. Увеличение размера атомов ведет к менее эффективному
перекрывание их атомных орбиталей и одновременно создает условия для одновременного
перекрывание орбиталей сразу многих атомов, т. е. к образованию многоатомных
молекул и атомных веществ, поэтому фосфор в обычных условиях, в отличие от
газообразного азота, - твердое вещество.
Фосфор в промышленности получают
восстановлением природных фосфатов коксом при температурах, близких к 1500 °С. Под
время охлаждения газообразных продуктов образуются сразу, минуя стадию
жидкости, кристаллы так называемого белого фосфора, кристаллическая решетка которого образована
молекулами Р4.
Эта алотропна модификация фосфора
химически очень активная. Уже при комнатной температуре белый фосфор окисляется
кислородом воздуха:
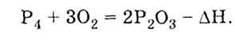
Таблица
Фосфор и его соединения
|
Фосфор
|
Соединения фосфора .
|
|
оксид фосфора (V)
|
ортофосфатная кислота
|
|
1. По
обычных условиях может существовать в виде двух алотропних модификаций: красный и
белый фосфор
2. Горит в кислороде
(проявляет восстановительные
свойства):
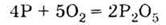
Белый
фосфор окисляется на воздухе при комнатной температуре:
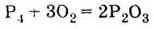
Получение
восстановлением
природного фосфата кальция с помощью кокса (углерод) и кварцевого песка SiO2
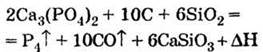
|
1. По
обычных условиях очень гигроскопичное твердое вещество белого цвета
2. Проявляет
свойства кислотных оксидов, взаимодействуя с водой:
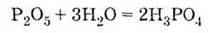
с щелочами:
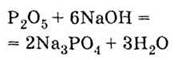
с
основными оксидами:
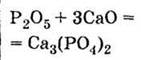
Получение
сжиганием
фосфора в избытке воздуха:
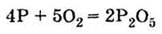
|
1. По
обычных условиях бесцветная твердое вещество, неограниченно растворимая в воде
2. Слабая трьохосновна кислота:
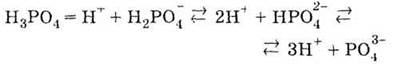
3. Взаимодействует со щелочами, основаниями и амфотерными
гидроксидами, а также аммиаком:
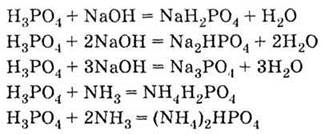
4. Взаимодействует с основными оксидами:
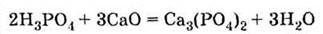
5. Взаимодействует
с фосфатом кальция, образуя дигидрофосфат (двойной суперфосфат):
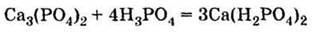
Получение
в промышленности
1) по реакции оксида фосфора (V) с водой:
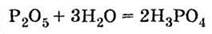
2) по реакции фосфата кальция с серной кислотой при
нагревании:
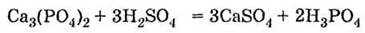
|
Своеобразие данной реакции заключается в
потому, что практически вся ее энергия выделяется в виде света, поэтому смеси,
которые имеют содержание белого фосфора, светятся на воздухе. Это явление
использовалось ранее, например, в процессе изготовления циферблатов и
стрелок часов и других приборов. Отсюда и название фосфора: «фосфорос» (от
греч. - то, что светится). На способности белого фосфора загораться при слабом
нагревании, в том числе от трения, было основано производство спичек. Но
именно поэтому они были очень опасны в обращении и становились причиной многих
несчастных случаев. К тому же высокая химическая активность белого фосфора обусловливает
его ядовитость.
Вторая алотропна модификация фосфора
- красный фосфор, который имеет атомную кристаллическую решетку, значительно менее реакционно
способен и поэтому не ядовитый. Полученный в результате реакции восстановления фосфата
белый фосфор превращают в красный нагреванием без доступа воздуха.
Красный фосфор используется в
современном производстве спичек (он входит в состав намазка на коробке). Но основная его
количество затрачиваемого на получение ортофосфатной кислоты по реакции:
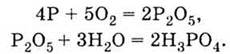
Безводная ортофосфатная кислота Н3РO4, в отличие от описанных в
предыдущих разделах кислот - газообразной НСl и жидких Н2SO4 и НNO3, - твердое бесцветное вещество, которое
смешивается с водой (как Н2SO4 и НNO3) практически во всех соотношениях.
В отличие от рассмотренных нами
раньше кислот - это относительно слабая кислота.
Ортофосфатная кислота трьохосновна и
поэтому диссоциирует ступенчато:
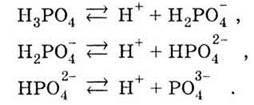
При
этом на каждом следующем ступени диссоциация происходит все в меньшей степени (в
тысячи раз). Например, в 1 М растворе Н3РO4 концентрация
ионов Н2РO4- равен 8 • 10-2 моль/л, НРO4
- 7 • 10-5 моль/л и РO43- - 1 •
10-8 моль/л.
Таким образом, при действии сильных кислот
на фосфаты - соли слабой кислоты - эта кислота и должна образовываться.
Вторым промышленным способом
получение ортофосфатной кислоты является обработка природных фосфатов серной
кислотой:
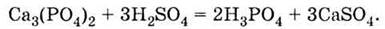
Химические свойства фосфора и его
соединений обобщены в таблице,
яка
приведенная выше.