УГЛЕРОД И ЕГО СОЕДИНЕНИЯ
ОКСИДЫ КАРБОНА
Имея четыре электрона на
внешнем энергетическом уровне, Карбон в соединении с Оксигеном, в зависимости от
условий, проявляет степени окисления +2 и +4.
Во время горения карбоновмісних
веществ (дрова, уголь, природный газ метан, спирт и др.) при температуре
обычного пламени проходит реакция:
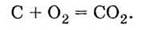
Но если создать условия для
повышение температуры (например, уменьшить теплоотдачу, что может происходить внутри
толстого слоя угля, который горит, в том числе в доменной печи), то протекают
реакции:
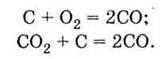
Продуктом полного сгорания углерода и
карбоновмісних веществ является оксид углерода (IV) СО2 - углекислый газ.
Он также образуется при дыхании живых организмов и гниения остатков.
Одновременно углекислый газ (вместе с водой) является основным веществом, которую потребляют
растения в процессе их роста.
При повышении давления уже за
комнатной температуры оксид карбона (IV) сжижается. Жидким СО2
заполняют некоторые типы огнетушителей.
При снижении давления жидкий оксид
карбона (IV) закипает. При этом его температура резко снижается, поскольку на
парообразования, как известно из физики, затрачивается большое количество теплоты. В
результате СО2 твердеет. В твердом виде (под названием «сухой лед»)
он применяется в качестве хладагента. При атмосферном давлении сухой лед» не
плавится, а подобно йода, фосфора, углерода перегоняется, только за значительно
низшей температуры (-75 °С).