СТРОЕНИЕ АТОМА
6. Волновая модель
6.3. Периодическая система элементов и волновая
модель
Порядок
расположение элементов в периодической системе можно объяснить на основе принципа
заполнение орбиталей. Электронную конфигурацию любого элемента можно
вывести, исходя из трех принципов, которые находятся в тесной связи с
учетом квантовых чисел.
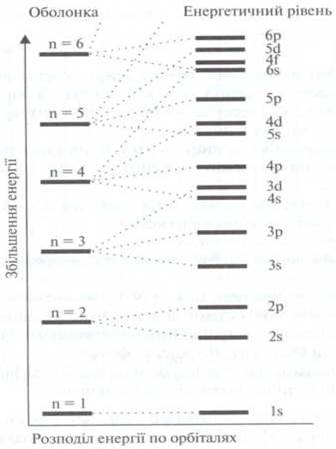
♦ Уровни с меньшей энергией заполняются в первую
очередь - принцип наименьшей энергии.
♦ Каждая орбиталь может быть занята максимум
двумя электронами с разным спіновим квантовым числом - принцип Паули.
♦ Орбитали с одинаковым побочным (орбитальным)
квантовым числом имеют одинаковую энергию и сначала заполняются электронами по
одном - правило Гунда.
|
Элемент
|
Конфигурация
электронов
|
Изображение
орбитали
|
|
Н
|
1s1
|

|
|
Не
|
1s2
|
|
Li
|
1s2
2s1
|
|
Ве
|
1s2
2s2
|
|
В
|
1s2
2s2 2p1
|
|
С
|
1s2
2s2 2p2
|
|
N
|
1s2
2s2 2p3
|
|
O
|
1s2
2s2 2p4
|
|
F
|
1s2
2s2 2p5
|
|
Ne
|
1s2
2s2 2p6
|
При
полном изображении электронной конфигурации атомов элементов полностью заняты
оболочки заменяют символом соответствующего инертного газа.
Пример.
Элемент Натрий, что стоит после инертного газа неона, имеет конфигурацию
электронов 
Периодическое
повторение аналогичных конфигураций электронов у различных элементов объясняет
периодичность появления элементов с подобными свойствами и образование групп, как,
например, щелочных металлов и галогенов.
Пример.
Все щелочные металлы по орбиталь с наибольшей энергией обладают одноелектронну s-орбиталь внешней оболочки.
Элементы
главных и побочных подгрупп
Элементы
в периодической системе подразделяются на элементы главных и побочных подгрупп.
Лантаноїди и актиноїди составляют отдельные группы элементов.
♦
В главных группах внешняя оболочка
элементов постепенно заполняется, а именно - от ns1 к ns2p6
- состояния, d- и
f-орбитали или пустые,
или полностью заняты.
♦ В побочных подгруппах в элементах происходит
заполнение d-орбиталей, эти
элементы называют также переходными элементами.
♦ В лантаноїдах и актиноїдах заполняются f-орбитали.
Запомните:
элементы главной группы имеют номер группы, который соответствует их числу валентных
электронов. Элементы побочных групп имеют разную валентность, поскольку в связях
могут принимать участие как электроны s- так и d-орбиталей,
которые имеют меньшую энергию.
Внимание:
число элементов в периоде не всегда соответствует максимальному заполнению
внешней оболочки электронами, которое, как известно, составляет 2n2.