Часть II.
НЕОРГАНИЧЕСКАЯ ХИМИЯ
Раздел 8. ВОДОРОД.
ГАЛОГЕНЫ
§
8.6. Хлор
Распространение в природе. В природе в
свободном состоянии хлор встречается только в вулканических газах. Очень распространены его
соединения. Важнейшие из них: хлорид натрия NaCl, хлорид калия КСl, хлорид магния МgСl2 ∙6Н2О, сильвинит,
состоит из NaCl и
КСl , карналлит
состав КСl ∙
МgСl2 ∙ 6Н2О, каинит
состав MgSO4 ∙ КСl ∙ 3Н2О и др.
Соединения хлора содержатся в водах
океанов, морей и озер. В небольших количествах они содержатся в растительных и
животных организмах. Хлор составляет 0,05 % массы земной коры.
Добывания. В лабораторных условиях хлор
добывают из соляной кислоты при взаимодействии ее с оксидом марганца(ИV). Реакция происходит при
нагревании:
4НСl + МnОr = Сl2 + МnСlr + 2Н2О.
Это окислительно-восстановительный процесс. НСl, точнее хлорид-ион Сl-, - восстановитель; МnОr - окислитель. Метод составления уравнения
реакции рассмотрены в § 7.3.
Вместо окисника МnОr можно применять перманганат
калия КМnВ4.
Тогда реакция будет происходить при обычной температуре, то есть без нагрева:
16НСl + 2КМnO4 = 5Сlr + 2МnСl2 + 2КСl + 8Н2O;
2Сl- - 2е- = Сl2 5;
+7
+2
Мn + 5е- = Мn
2,
В промышленности хлор получают
электролизом концентрированного раствора хлорида натрия. Хлор выделяется на аноде.
При этом образуются также водород (выделяется на катоде) и гидроксид натрия
(остается в растворе).
Сжиженный хлор (сжижается за
комнатной температуры при давлении 600 кПа) хранят в стальных баллонах и в
таком виде доставляют к месту использования.
Физические свойства. Хлор - ядовитый
газ желто-зеленого цвета с резким запахом. Тяжелее воздуха в 2,5 раза. При
20°С в 1 объеме воды растворяется 2,3 объема хлора.
Раствор хлора в воде называется
хлорной водой. Хлор хорошо растворяется в органических растворителях.
Хлор вызывает раздражение дыхательных
путей, а вдыхание больших количеств его приводит к смерти от удушья.
В природном хлоре содержатся два
изотопы: 3517Сl (75,4 %) и 3717Сl (24,6 %).
Химические свойства. Молекула хлора
состоит из двух атомов, характер связи в ней ковалентная неполярная:
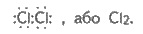
Сильные окислительные свойства хлор
проявляет при взаимодействии с металлами. При этом атомы металла отдают электроны,
а молекулы хлора их присоединяют. Например:
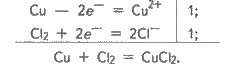
Хлор
взаимодействует со многими неметаллами. Например:
2Р + ВСl2 = 2РСl3;
2Р + 5Сl2 = 2РСl5.
Своеобразно реагирует хлор с водородом. В
темноте смесь хлора с водородом не взаимодействует. Однако при сильном освещении
реакция происходит очень быстро, со взрывом:
Сl2 + Н2 = 2НСl.
На самом же деле, как показали
исследования, эта реакция происходит значительно сложнее. Молекула Сl2 поглощает квант света h
v и расщепляется на
атомы (неорганические радикалы Сl)
(см. также § 16.3). Это является началом реакции (начальное возбуждение реакции). Потом
она продолжается сама собой. Каждый из
атомов-радикалов хлора Сl
реагирует с молекулой водорода. При этом образуются Н° и НСl. В свою очередь, атом-радикал
водорода Н взаимодействует с молекулой Сl2, образуя НСl и Сl, и т. д. Наглядно это можно
изобразить схемой:
Сl2 + h v = Сl + Сl;
Сl + Н2 = НСl
+ Н°;
Н° + Сl2 = НСl + Сl и т. д.
Начальное возбуждение повлекло
цепь последовательных реакций. Такие реакции называются цепными. Вследствие
цепной реакции хлора с водородом образуется хлороводень.
Как установил М. М. Семенов,
цепные реакции очень распространены и происходят из-за образования и следующую
взаимодействие свободных атомов или групп атомов - радикалов. Они играют большую
роль во многих важных химических процессах (процессы горения, взрыва, полимеризации
т.п.).
Если поджечь струю водорода, что
получается, например из прибора Кіппа, и пропустить его в стакан с хлором, то
водород будет гореть в нем голубым пламенем с образованием хлороводорода.
От органических соединений хлор отбирает
гидроген, а карбон остается в свободном состоянии. Поэтому такие вещества, как
скипидар, парафин, сгорают в хлоре с выделением большого количества копоти и
хлороводорода.
Хлор замещает водород в насыщенных
углеводородах и присоединяется к ненасыщенным соединениям:
СН4 + Сl2 = СН3Сl + НСl;
С2Н4 + Сl2 = С2Н4Сl2.
Он вытесняет бром и йод из их соединений
с гідрогеном и металлами:
Сl2 + 2KBr = 2КСl + r2.
Хлор взаимодействует с водородом с образованием
двух кислот - соляной (сильная кислота) и хлоратної(l) (слабая кислота).
Реакция обратима:
Сl2 + Н2O⇆НСl + HClO,
в ионной форме
Сl2 + Н2O⇆Н+
+ Сl-
+ НСlО.
Хлоратна(и)
кислота очень неустойчива. При нагревании или на свету она разлагается на
хлоридную кислоту и кислород: 2НСlO
= 2НСl
+ O2.
Хлоратна(И) кислота - сильный
окислитель. Образованием объясняются ее отбеливающие свойства хлора при наличии
влаги (воды). Сухой хлор не отбеливает.
Хлор непосредственно не взаимодействует с
кислородом, азотом и углем (их соединения получают косвенным путем). Если нет
влаги, то хлор не взаимодействует с железом. Это дает возможность хранить его в
стальных баллонах и цистернах.
Применение. Хлор применяется
для обеззараживания питьевой воды (хлорирование воды), отбеливания тканей и бумажной
массы. Большие количества расходуются для получения соляной кислоты,
хлорной извести, а также различных химических соединений, содержащих хлор.