Часть II.
НЕОРГАНИЧЕСКАЯ ХИМИЯ
Раздел 8. ВОДОРОД.
ГАЛОГЕНЫ
§ 8.5. Общая характеристика
подгруппы галогенов
Во время рассмотрения элементов по химии
подгруппами исключительно важно уметь использовать прогнозирующую роль
периодического закона и периодической системы элементов Д.И. Менделеева. Тогда
многие свойства элементов и их соединений можно описать, не пользуясь
учебниками. Так, по положению элемента в периодической системе можно описать
строение атома - заряд и состав ядра и электронную конфигурацию, по последней
-
определить степени окисления элемента в соединениях, возможность образования молекулы
при обычных условиях, тип кристаллической решетки простого вещества в твердом состоянии.
Наконец, можно определить формулы высших оксидов и гидроксидов элементов, изменение
их кислотно-основных свойств по горизонтали и вертикали периодической
системы, а также формулы различных бинарных соединений с оценкой характера химических
связей. Это значительно облегчает изучение свойств элементов, простых веществ и
их соединений. Начинать следует с рассмотрения общей характеристики каждой
подгруппы.
В подгруппу галогенов входят фтора,
хлор, бром, йод и астату (астату - радиоактивный элемент, изучен мало). Это p-элементы VII группы периодической
системы Д. И. Менделеева. На внешнем энергетическом уровне их атомы имеют по
7 электронов ns2 nг5
(табл. 8.1). Этим объясняется сходство их свойств.
Они легко присоединяют по одному электрону,
проявляя степень окисления - 1. Такая степень окисления галогены проявляют в
соединениях с гідрогеном и металлами.
Таблица
8.1. Свойства элементов подгруппы галогенов
|
Свойство
|
F
|
Сl
|
Вr
|
l
|
At
|
|
1.
Порядковый номер
|
9
|
17
|
35
|
53
|
85
|
|
2.
Валентные электроны
|
2s22p5
|
3 s2
3г5
|
4s24p5
|
5s25
г5
|
6s26p5
|
|
3.
Энергия ионизации атома, эв
|
17,42
|
12,97
|
11,84
|
10,45
|
9,20
|
|
4.
Относительная электроотрицательности
|
4,1
|
2,83
|
2,74
|
2,21
|
1,90
|
|
5. Степень
окисления в соединениях
|
-
1
|
-1,+
1, +3,+5, +7
|
-1.+
1, +3,4-5, +7
|
-1.+
1, +3,+5, +7
|
-1.+
1, +3,+5, +7
|
|
6. Радиус
атома, нм
|
0,0064
|
0,099
|
0,114
|
0,133
|
-
|
Однако атомы галогенов, кроме фтора, могут
проявлять и положительные степени окисления: +1, +3, +5, +7. Возможные значения
степеней окисления объясняются электронному строению атомов, которую в атома фтора
можно изобразить схемой:
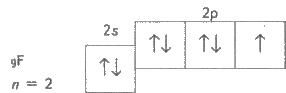
Как наиболее электроотрицательный
элемент, фтора может присоединить только один электрон на 2р-подуровень. У него
один неспаренный электрон, поэтому фтора бывает только одновалентним, а его степень
окисления всегда-1.
Электронное строение атома хлора
изображается схемой:
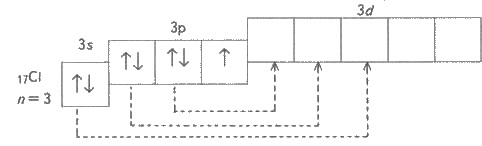
У атома хлора один неспаренный
электрона на 3р-подуровне, и в обычном (невозбужденном) состоянии хлор
одновалентний. Но поскольку хлор находится в третьем периоде, то у него есть
еще пять орбиталей 3d - підрівня,
на которых могут расположиться 10 электронов.
В возбужденном состоянии атома хлора
электроны переходят с 3р - и Сs-подуровней
на 3d- підрівень
(на схеме показано стрелками). Разъединение (розпаровування) электронов,
находятся на одной орбитали, увеличивает валентность на две единицы. Очевидно,
хлор и его аналоги (кроме фтора, могут проявлять лишь нечетную переменную
валентность 1, 3, 5, 7 и соответствующие положительные степени окисления. У фтора нет
свободных орбиталей, а следовательно, во время химических реакций не происходит разъединение
спаренных электронов в атоме (см. электронное строение атома фтора). Поэтому,
рассматривая свойства галогенов, всегда следует учитывать особенности фтора и
его соединений.
Водные растворы водородных соединений
галогенов являются кислотами: HF -
фтороводнева, или фторидна плавиковая), НСl - хлороводнева (соляная), или
хлоридная, НВr
- бромоводнева, или бромідна, Нl
- йодоводнева, или йодидна.
Следует иметь в виду, что кроме общих
свойств галогены имеют и различия. Это особенно характерно для фтора и
его соединений. Сила кислот в ряду возрастает, что объясняется уменьшением в этом
самом направлении энергии связи HR (где R - элемент). Плавиковая кислота
самое слабое в этом ряду, поскольку энергия связи Н - F здесь наибольшая. В такой же
последовательности уменьшается и прочность молекулы НГ (где Г - галоген), что обусловлено
увеличением між'ядерної расстояния (см. табл. 8.1, п. 6). Растворимость
малорастворимых солей уменьшается в ряду АgСl - АgВr - Аgl; в отличие от них соль AgF
хорошо растворяется в
воде.
Фтора крепко удерживает электроны
(см. табл. 8.1, п. С, 4), у него степень окисления (-1) (см. табл. 8.1,
п. 5). Фтор иначе взаимодействует с водой, чем хлор: разлагает воду с образованием
фтороводню, фторида кислорода(II), пероксида водорода, кислорода и озона:
F2 + Н2О = 2HF
+ О; 2O
= А2; А 3 = А3;
O + F2 = F2O; Н2O + О = Н2О2.
Уравнение реакции взаимодействия хлора с
водой см. § 8.6.
Пункты 3 и 6 табл. 8.1
характеризуют неметаллические свойства элементов. Поскольку радиус атома
растет, а энергия ионизации уменьшается в ряду F - At ослабляются неметаллические
свойства. Сильнее всего они выражены у фтора.
Реакционная способность галогенов
ослабляется в ряду F -Сl - r - l. Поэтому предыдущий элемент способен
вытеснять следующий из кислот типа НГ (Г - галоген) и их солей. В этом случае
активность
F2 > l2 > r2 > l2.
Закономерно изменяются физические
свойства галогенов с увеличением порядкового номера: фтор - газ, что трудно
сжижается, хлор - газ легко сжижается, бром - жидкость, йод - твердое
вещество.