ОКИСЛЕНИЯ
И ВОССТАНОВЛЕНИЕ
4. Электролиз
Электролиз
- это обратный процесс окислительно-восстановительной реакции, спонтанно протекает в
батареи. При использовании электрической энергии принудительно вызывают процесс
окислительно-восстановительной реакции. В то же время электрическая энергия превращается в химическую
энергию.
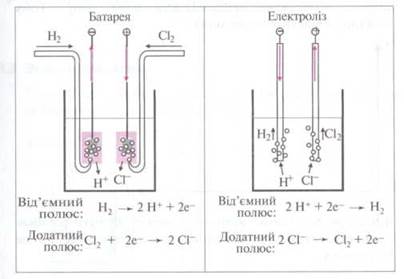
В
обоих случаях электрод, на котором происходит окисление, называется анодом
(анодный протектор). Электрод, на котором происходит восстановление, называют
катодом.
В
батареи анод - отрицательный полюс, а катод - положительный.
При
электролизе анод - положительный полюс, а катод - отрицательный.
4.1. Напряжение разложения
При
электролизе ионы электролита осаждаются на электродах и там разряжаются.
Вещества, которые образуются во время процесса, оседают на электродах и вместе с
электролитом образуют / гальванический элемент, полюса которого противоположны
полюсов приложенного напряжения.
В соответствии
к вольт-амперной характеристики процесса электролиза при небольшом значении
напряжения ток практически не проходит, поскольку приложенное напряжение и напряжение
поляризации нейтрализуют друг друга. Поэтому электролиз происходить не может.

Только
при достижении определенного значения напряжения начинает проходить ток и происходит
выделение веществ на электродах.
Для
проведение электролиза нужно преодолеть порог минимального напряжения. Это напряжение
называют напряжением разложения. Она соответствует сумме окислительно-восстановительных потенциалов,
приложенные к электродам.
Пример.
При электролизе раствора купрум(ІІ) хлорида оседает медь и выделяется хлор.
Отрицательный
электрод (катод): Сu2+
+ 2 е-
→
Cu.
Положительный
электрод (анод): 2 Сl- →
Сl2
+ 2 е-.
Напряжение
расписания U0, что
нужна для протекания процесса электролиза, является разностью стандартных потенциалов
окислительно-восстановительных пар Cu/Cu2+ и 2 Сl-/Сl2.
U0= 1,36 В - 0,35 В = 1,01 В.
Часто
для электролиза нужна минимальная напряжение, которое существенно превышает расчетную
напряжение разложения. Такое превышение напряжения расписания называют перенапряжением. Ее
величина в значительной степени определяется
♦ выбором материала электродов;
♦ свойствами вещества, оседает.