ЭЛЕКТРОЛИТЫ
РЕАКЦИИ В РАСТВОРАХ ЭЛЕКТРОЛИТОВ
В растворах электролитов в химическую
взаимодействие вступают ионы. Выясним, в каких случаях это происходит.
Если смешать водные растворы поваренной
соли (хлорида натрия) и известковой воды (раствора гидроксида кальция), то
внешних изменений не наблюдается. Формально можно написать
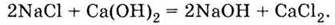
Учитывая то, что все четыре
вещества (хлорид и гидроксид натрия, хлорид и гидроксид кальция) - свободные
электролиты, запишем уравнение реакции в ионном виде:
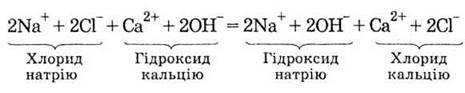
Чем левая часть этого уравнения
отличается от правой? Ничем, кроме порядка написания формул. Исходная смесь ионов
не изменилась. Никакой химической реакции не произошло.
Если хлорид натрия заменить на
карбонат натрия, то при смешивании их растворов выпадает осадок, происходит
реакция. В ионном виде ее уравнение можно записать так:
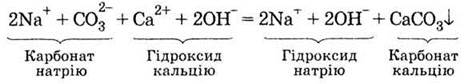
Если не указывать ионы, которые не приняли
участия в реакции (это ионы Nа+ и ОН-), то получим запись, называется
сокращенным ионным уравнением реакции:
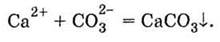
Сокращенное ионное уравнение отражает,
что на самом деле происходит в растворе. Например, в данном случае оно показывает:
если в раствор одновременно попадают ионы Са2+ и СO32-, независимо от того, в состав которых
веществ они входили и при диссоциации каких веществ образовались, то происходит
реакция образования карбоната кальция СаСO3.
Эта реакция происходит потому, что ионы,
которые соединяются, образуют малорозчинну вещество, которое выпадает в виде осадка,
то есть выходит из сферы реакции. Это первый пример необратимой реакции в
растворе электролита.
Другой пример - взаимодействие карбоната
натрия с хлоридной кислотой. Запишем уравнение электролитической диссоциации
взятых веществ:
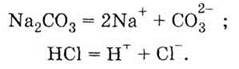
В этом растворе следует принимать во внимание
возможность взаимодействия только разноименно заряженных ионов. Ионы Nа+ не могут взаимодействовать
с ионами Сl-, потому что возможна соединение NаСl - соль, которая является сильным электролитом и в растворе существует
только в виде отдельных ионов Nа+ и Сl-. Могут взаимодействовать ионы СО32-
и Н+ с образованием слабого (то есть малодисоційованої)
карбонатной кислоты:
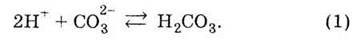
Карбонатная кислота - очень неустойчивая
соединение и практически мгновенно разлагается на воду и кислотный оксид:
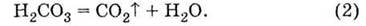
Диоксид углерода - углекислый газ
покидает сферу реакции. При добавлении уравнений (1) и (2) получаем суммарный запись
уравнение реакции карбонат-ионов с ионами Водорода:
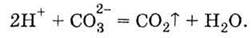
Газ, который покидает сферу реакции, не
может вступить в обратную реакцию, следовательно, это необратимая реакция. Таким образом,
реакция карбоната натрия с хлоридной кислотой может быть подана молекулярным
уравнением
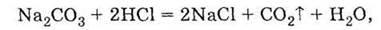
полным
ионным уравнением
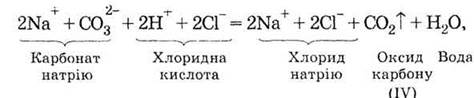
сокращенным
ионным уравнением
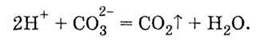
Последнее уравнение, как и все сокращенные
ионные уравнения, отражающего суть рассматриваемой химической реакции: независимо от
вещества, которая содержит карбонат-ионы, и кислоты во время их взаимодействия всегда будет
выделяться углекислый газ и образовываться вода. (Однако кислота должна быть не
слабее карбонатной, т.е. содержать в своем растворе больше ионов Водорода, чем
карбонатная.)
Таким образом, говоря о химизм
процесса, следует пользоваться сокращенным ионным уравнением реакции. В то же время в
процессе расчетов количеств веществ, вступивших в реакцию и образовавшихся
необходима запись в молекулярной форме.
Вода и другие слабые электролиты в ионных
уравнениях реакций, обычно, записываются в молекулярном виде и только в
отдельных случаях - в ионном.
Следовательно, если в результате реакции
образуется вода, то из сферы реакции получаются некоторые участники реакции, а именно ионы
Н+ и ОН-, а это, собственно, и является необходимым условием
необратимости химического взаимодействия.
Это еще один пример необратимых
реакций - реакции нейтрализации, то есть взаимодействия между кислотами и основаниями. Ионное
уравнение реакции, которая происходит, необходимо записать так:
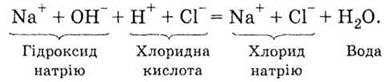
Из раствора исчезают ионы Н+
и ОН-, как это видно из сокращенного ионного уравнения:
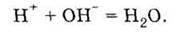
Итак, чтобы в растворе электролита
произошла реакция (а она происходит при участии ионов), необходимо, чтобы хоть
некоторые ионы вышли из сферы реакции. Это реализуется при выпадении осадка,
выделении газа, образовании слабого электролита (очень часто воды).