ЭЛЕКТРОЛИТЫ
СИЛЬНЫЕ И СЛАБЫЕ ЭЛЕКТРОЛИТЫ
Если реакция вещества с водой, которая
приводит к образованию ионов, не проходит до конца и в растворе остаются
молекулы исходного вещества, то есть процесс электролитической диссоциации обратим,
то такое вещество относится к слабым электролитам.
Кроме описанных в предыдущем
параграфе воды и аммиака, к слабым электролитам относятся почти все
малорастворимые в воде основания (щелочи), например, гидроксид купруму (II):
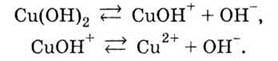
Некоторые кислоты - тоже слабые
электролиты, например, карбонатная:
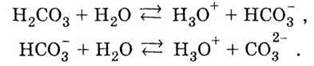
Слабыми электролитами являются все кислоты,
которые используют в еде (уксусная, лимонная, яблочная и т. д.) или как лекарство (борная,
аскорбиновая - витамин С, ацетилсалициловая аспирин и др.).
Слабые электролиты, которые являются основами и
содержат два или больше гидроксид-ионы, а также багатоосновні кислоты диссоциируют
ступенчато, причем обратимо по каждому щаблеві, как это показано выше для
диссоциации гидроксида купруму и карбонатной кислоты. Отщепление первого иона
(диссоциация по первой ступени) происходит от нейтральной молекулы (ОН-
от Сu(ОН)2, Н+ от
Н2СO3), а второго иона (диссоциация на
второй ступени) - от противоположно заряженного иона (ОН- от СuОН+, Н+ от НСO3-). Очевидно, что отщепление второго иона
происходит тяжелее, и, соответственно, диссоциация по второй ступени протекает в
тысячи и десятки тысяч раз слабее, чем на первом.
Сильными электролитами называются
вещества, молекулы которых в растворе отсутствуют. Диссоциация сильных электролитов
протекает необратимо. К таким электролитам относятся большинство солей (практически
все, о которых упоминается в учебнике), щелочи (растворимые в воде основания), а также
сильные кислоты (хлоридная, сульфатная, азотная). Уравнения электролитической
диссоциации сильных электролитов записываются со знаком равенства:
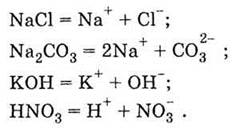
Таким образом, сильные и слабые
электролиты различают по характеру их диссоциации: обратимо диссоциируют слабые
и необратимо - сильные электролиты. Кроме этого, слабые электролиты диссоциируют
ступенчато.