ЭЛЕКТРОЛИТЫ
КИСЛОТЫ КАК ЭЛЕКТРОЛИТЫ
Свойства кислот могут быть
поделены на три группы.
Первая группа объединяет общие
свойства кислот обусловлены наличием в их растворах ионов Водорода. Это -
изменение окраски индикаторов, вкус, взаимодействие с металлами, стоящими в ряду
напряжений металлов левее Водорода, с основными оксидами, щелочами и основаниями.
Приведем соответствующие сокращенные ионные
уравнение:
с
металлами 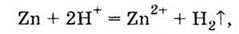
с
основными оксидами 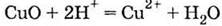
с
щелочами 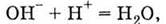
с
нерастворимыми основаниями 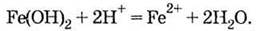
Ко второй группе можно отнести реакции,
обусловленные свойствами кислотных остатков. Это - специфические для каждой кислоты
реакции. За ними кислоты можно различить между собой. Во многих таких реакциях
образуются малорастворимые, иногда окрашенные соли.
Например, для серной кислоты Н2SO4 - это реакции с растворами соединений
бария (гидроксидом, солями):
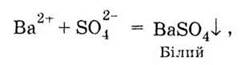
для
соляной кислоты НСl - это реакции с растворами солей
арґентуму, например АgNO3:
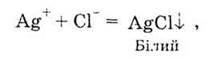
для
карбонатной кислоты Н2СO3 - с растворами соединений кальция:
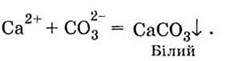
Третью группу составляют реакции,
протекание которых обусловлено свойствами собственно молекул кислот, такими, как сила
кислоты, ее растворимость в воде, прочность молекулы, легкость. Приведем примеры.
Сильная кислота вытесняет более слабую из ее
солей:
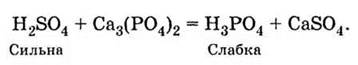
Реакция проходит потому, что
образуется слабый электролит Н3РO4.
Нелетка кислота вытесняет летучее: