ЭЛЕКТРОЛИТЫ
ОБРАТИМЫЕ РЕАКЦИИ
Реакция диссоциации воды, уравнение
которой приведены в предыдущем параграфе, протекает в незначительной степени. С каждого
миллиарда молекул воды в ней принимают участие только две, поэтому концентрация каждого из
ионов, которые образуются, ничтожно мала (10-7 моль/л).
Когда говорят, что вода - слабый
электролит, то имеют в виду, что она слабо диссоциирует на iоны. Кроме воды существует много других
слабых электролитов, степень диссоциации которых, т.е. доля молекул,
продисоціювала, незначительна. В таких растворах электролитов устанавливается химическая
равновесие, при котором скорость диссоциации равна скорости ассоциации:
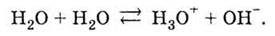
В упрощенной форме его можно
записать так:
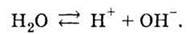
Реакции, которые не проходят до конца,
то есть ведут к установлению равновесия, называются оборотными. Для обозначения
оборачиваемости в уравнении реакции вместо знака равенства используют знак «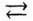 ».
».
Реакция диссоциации воды является обратимой.
Другой пример обратимой реакции - взаимодействие воды с аммиаком.