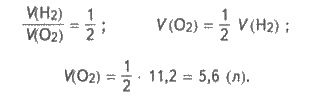Часть И. ОБЩАЯ
ХИМИЯ
Раздел 7.
ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦІЇ.ЕЛЕКТРОЛІЗ
§
7.9. Решение типовых задач
Окислительно-восстановительные реакции
Задача
1. Подберите
коэффициенты в схеме окислительно-восстановительной реакции:
S + HNO3
-> H2SO4 +
NO.
Решения. Коэффициенты находим
методом электронного баланса. Отметим степени окисления элементов, которые их
меняют:
0
+5 +6
+2
S + HNO3 -> H2SO4 + NO,
S
- восстановитель, a
HNO3 -
окислитель.
Составляем электронные уравнения и
находим коэффициенты у окисника, восстановителя и продуктов их восстановления и
окисления:
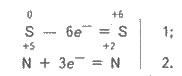
Подставим
найденные коэффициенты в схему реакции:
S+ 2HNO3 = H2SO4 + 2NO.
Проверяем правильность написания
уравнение реакции. Число атомов каждого элемента в левой части уравнения
равен числу тех самых атомов в правой части уравнения. Следовательно, уравнение
составлено правильно.
Задача 2. Составьте уравнение реакции
восстановление Fе3O4 водородом.
Решения. Записываем схему процесса
с указанием изменения степеней окисления элементов:
+8/3
0
0
+1
Fe3O4 + Н2 -> Fe
+ Н2О.
Составляем
электронные уравнения:
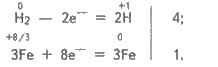
Найденные коэффициенты подставляем в
схему процесса, заменяя стрелку знаком равенства:
Fe3O4 + 4Н2 = 3Fe
+ 4Н2О.
Задача 3. Подберите коэффициенты в схеме
окислительно-восстановительной реакции:
KNO2 + К2Сr2O7 + H2SO4 ->КNО3 + Cr2(SO4)3
+ K2SO4 + Н2О.
Решение 1. Находим коэффициенты
методом электронного баланса. Записываем схему реакции с указанием степени
окисления элементов, которые его меняют:
+3
+6
+5
+3
KNO2
+ К2Сr2O7 + H2SO4
-> KNO3 + Cr2(SO4)3
+ K2SO4
+ Н2O.
Здесь KNO2 является восстановителем, а дихромат калия - окисником.
Составляем электронные уравнения, учитывая, что 1 моль Cr2(SO4)3
и 1 моль К2Сr2О7 содержат по 2 моль
атомарного хрома:
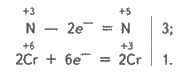
Найдены коэффициенты у восстановителя
KNO2 и продукта его окисления KNO3 и у окисника К2СrO7 и продукта его восстановления Cr2(SO4)3 подставляем в схему
реакции:
3KNO2
+ К2СrO7 -> 3KNO3
+ Cr2(SO4)3
+ K2SO4
+ 4Н2О.
Остальное коэффициентов находим в
последовательности: соль (K2SO4), кислота (H2SO4), вода. Окончательное уравнение реакции
будет иметь вид:
3KNO2 + К2Сr2О7 + 4H2SO4 = 3KNO3 + Cr2(SO4)3 + K2SO4 + 4Н2O.
Для проверки правильности
коэффициентов подсчитываем число атомов кислорода в левой и правой частях
уравнения. В левой части: 3∙2 + 7 + 4∙ 4 = 29. В правой части: 3
∙ 3 + + 3 4
+ 4 + 4 = 29.
Решение 2. Находим коэффициенты
методом напівреакцій (факультативно) .
В первой напівреакції восстановитель -
нитрит-ион NO2 - переходит в нитрат-ион NO-3, принимая один атом кислорода от
молекулы воды:
NO-2 + Н2O -> NO-3 + 2Н+.
Сравняв число зарядов, получим:
NO-2 + Н2О - 2е- ->
NO-3 + 2Н+.
В
второй напівреакції окислитель - ион Сr2O2-7
- переходит в ион Сr3+, то есть 7 атомов кислорода в кислой среде
связываются с 14 ионами водорода с образованием воды:
Сr2O2-7 + 14Н+ -> 2Сr3+ + 7Н2O.
Сравняв число зарядов, получим:
Сr2O2-7 + 14Н+ + 6е-
= 2Сr3+ + 7Н2О.
Составляем суммарное ионное уравнение
реакции:

3NO-2
+ 3H2O + Cr2O2-7 + 14H+ = 3NO-3
+ 6Н+ + 2Cr3+
+ 7Н2O.
Сократив
одинаковое число ионов водорода и молекул воды в левой и правой частях
уравнение, получим:
3NO-2 + Сr2O2-7 + 8Н+ = 3NO-3 + 2Cr3+ + 4Н2О.
Добавляя
одинаковое число ионов в левой и правой частей уравнения, получаем уравнение
реакции в молекулярной форме:
3NO-2 + Сr2О2-7 + 8Н+
= 3NO-3 +
2Сr3+ + 4Н2O;
ЗК+ + 2К+ + 4SO2- = 3К+ + 3SO2-4+ 2К+ + SO2-4;
KNO2
+ К2Сr2О7 + 4H2SO4
= 3KNO3
+ Cr2(SO4)3
+ K2SO4
+ 2Н2О.
Задача 4.
Подберите коэффициенты в окислительно-восстановительной реакции с участием органических соединений:
СН3ОН + KMnO4 + H2SO4 -> НСООН + MnSO4 + K2SO4 + Н2О.
Решения.
Составляем схему реакции с указанием степеней окисления атомов в молекулах восстановителя,
окисника и продуктов их восстановления и окисления:
-2
+7 +2
+2
СН3ОН
+ KMnO4 +
H2SO4 ->
НСООН + MnSO4.
Отсюда
видно, что СН3ОН - восстановитель, а КМnO4 - окислитель. Составляем электронные
уравнение:
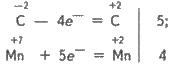
и
подставляем коэффициенты в схему реакции:
5СН3ОН + 4КМnO4 + H2SO4 -> 5НСOOН + 4MnSO4 + K2SO4 + Н2О.
Остальные
коэффициентов находим подбором в обычной последовательности: K2SO4, H2SO4, Н2О. Окончательное уравнение
реакции будет иметь вид:
5СН3ОН
+ 4КМnO4 + 6H2SO4 -> 5НСOOН + 4MnSO4 + +2K2SO4+11H2O.
Электролиз
расплавов и растворов
Задача 1. Составьте схему электролиза
расплавов: а) гидроксида калия; б) сульфата натрия.
Решение, а) В расплаве гидроксид
калия диссоциирует на ионы:
КОН = К+ + ОН-.
Во время прохождения сквозь расплав
электрического тока к отрицательному электроду (катоду) будут переходить катионы
К и присоединять электроны (восстанавливаться). К положительному электроду (аноду)
будут поступать анионы OН-
и отдавать электроны (окиснюватися). Итак, схема процесса приобретает такого
вид:
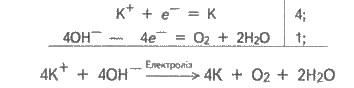
или

б) Сульфат натрия в
расплаве диссоциирует на ионы: Na2SO4 ⇆2Na+ + SO2-4 .
Схема
процесса электролиза:
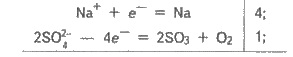
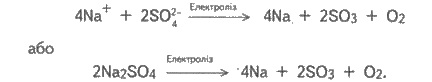
Задача 2. Составьте схемы электролиза водных
растворов: а) сульфата купруму(II); б) хлорида магния; в) сульфата калия. Во всех
случаях электролиз проводится с использованием угольных электродов.
Розв'язання. а) В растворе сульфат
купруму(II) диссоциирует на ионы:
CuSO4 ⇆Cu2+ + SO2-4.
Ионы купруму(II) могут
восстанавливаться на катоде в водном растворе. Сульфат-ионы в водном растворе не
окисляющиеся, поэтому на аноде будет происходить окисление воды (см. § 7.7). Схема
электролиза:
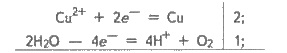

или
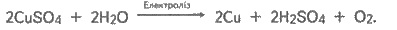
б) Диссоциация хлорида магния в
водном растворе:
МgСl2 ⇆Мg2+ + 2Сl-.
Ионы магния не могут восстанавливаться
в водном растворе (происходит восстановление воды), хлорид-ионы - окисляющиеся
(см. § 7.7). Схема электролиза:
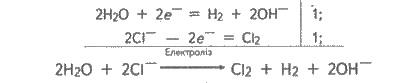
или

в) Диссоциация сульфата калия в
водном растворе:
K2SO4 = 2К+ + SO2-4.
Ионы калия и сульфат-ионы не могут
разряжаться на электродах в водном растворе (см. § 7.7), следовательно, на катоде
будет происходить восстановление, а на аноде - окисление воды. Схема электролиза:
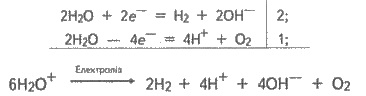
или,
учитывая, что 4Н+ + 4OН = 4Н2О (осуществляется при перемешивании),
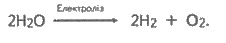
Задача 3. Во время электролиза водного раствора
гидроксида калия с инертными электродами на катоде выделился водород объемом
11,2 л (нормальные условия). Рассчитайте объем кислорода, который выделился при этом на
аноде.
Решение 1. Записываем уравнение
электролиза, учитывая, что на катоде восстанавливается вода (катионы калия не
восстанавливаются при электролизе водных растворов), а на аноде окисляющиеся
гидроксид-ионы:
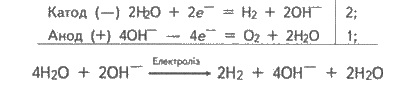
или

Определяем
количество вещества водорода, выделившегося:
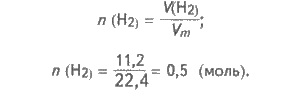
С
уравнения реакции следует, что

Вычисляем объем кислорода,
выделился:
V(O2) = n(O2) Vm; V(O2) = 0,25 • 22,4 = 5,6 (л).
Решение 2. Используем
следствие из закона Авогадро, согласно которому одинаковые количества веществ различных
газов при одинаковых условиях занимают одинаковые объемы. Поэтому из уравнения электролиза
(см. решение 1) получим: