ОКИСЛЕНИЯ
И ВОССТАНОВЛЕНИЕ
3. Электрохимия
3.3.
Батареи
Батарея
состоит из трех частей:
♦ отрицательный электрод, который отдает электроны при
прохождении тока, то есть окисляется;
♦ положительный электрод, получает электроны при
прохождении тока, то есть восстанавливается;
♦ электролит, который имеет хорошую электрическую
проводимость и поэтому обеспечивает низкий / внутреннее сопротивление батареи.
Пример.
Широко применяемая батарея - щелочная / марганцевая батарея. Напряжение между полюсами
составляет 1,5 В.
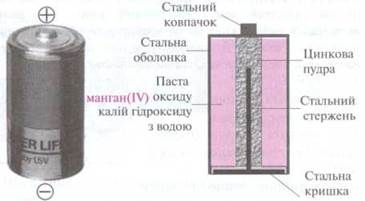
Электролит
- это щелочной раствор калий гидроксида, положительный электрод - манган(ИV) оксид, отрицательный электрод -
цинковый.
Отрицательный
электрод: Zn →
Zn2+ + 2е-.
Положительный
электрод: 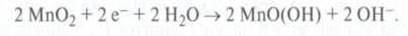
Роль электролита
Ионы
Цинка и гидроксид-ионы, которые образуются во время окислительно-восстановительного процесса,
диффундируют в электролит и образуют малорастворимый цинк гидроксид, который снижает
ведущую способность электролита. Однако высокая концентрация гидроксид-ионов
предотвращает образование этого продукта и соответственно быстрому увеличению
внутреннего сопротивления:
Zn2+ + 2 ОН- →
Zn(OH)2
важкорозчинний
Zn(OH)2 + 2 ОН- →
[Zn(OH)4]2- легкорозчинний
Запомните:
электролит не принимает участия в окислительно-восстановительной реакции, но реагирует с продуктами
реакции и влияет на срок службы батареи.