ОКИСЛЕНИЯ
И ВОССТАНОВЛЕНИЕ
3. Электрохимия
3.2.
Электрохимический ряд напряжений металлов
Чтобы
использовать окислительно-восстановительную реакцию, которая проходит между металлом и ионами
менее активного металла, для получения электрической энергии, также нужно
провести пространственное разделение «партнеров» окислительно-восстановительной реакции.
Пример.
Если пластинку железа поместить в раствор, содержащий ионы Железа, а медную
пластинку в раствор, содержащий ионы Купруму, то между двумя металлами возникнет
электрическая напряжение. Если проводником соединить пластинки, которые являются двумя полюсами,
с электрическим прибором, то от железа к меди будет проходить электрический ток.
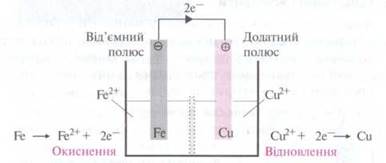
Металлы,
погруженные в раствор одноименных ионов, образуют гальванический полуэлемент. Они
имеют определенную способность отдавать электроны и переходить в раствор как ионы.
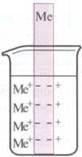
Соответствующие
ионы металлов стремятся в свою очередь получить электроны и осесть в решетку
металлов.
Поэтому,
если опустить металл в раствор соли, содержащей соответствующие ионы металлов, то между
металлом и ионами этой сопряженной окислительно-восстановительной пары устанавливается
равновесие реакции:
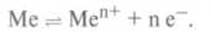
По
одинаковый промежуток времени в раствор переходит столько атомов металлов, что отдали
электроны, сколько ионов металлов, которые приняли электроны, перешедшие в металлическую
решетку.
Поэтому
на границе между металлом и раствором образуется двойной электрический слой, который
можно сравнить с заряженным конденсатором.
Разницу
зарядов в граничном слое называют электродным потенциалом, который имеет определенное
значение для каждой окислительно-восстановительной пары, состоящей из металла и связанного
иона металла.
Запомните:
электродный потенциал зависит от вида окислительно-восстановительной пары и от
концентрации ионов в растворе. Окислительно-восстановительные (электродные) потенциалы
недоступны для прямого измерения. Поэтому для сравнения используют другую
окислительно-восстановительную пару и определяют разность потенциалов.
По
точку отсчета для сравнения электродных потенциалов используют равновесие
между элементарным водородом и ионами гідроксонію (упрощенно Н+):
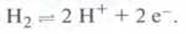
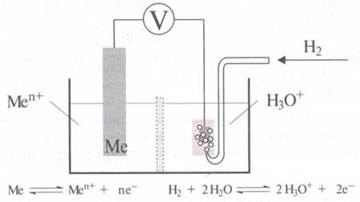
Этот
так называемый стандартный водородный электрод является платиновой пластинкой, которая омывается
газообразным водородом, которая погружена в раствор кислоты с концентрацией с(Н3О+)
= 1 моль/л при температуре Т = 298 К (= 25 °С).
Окислительно-восстановительный
потенциал стандартного водородного электрода принято считать равным нулю Е0Н = 0 В.
Разную
способность металлов переходить в раствор путем отдачи электронов выражают
электрохимическим рядом напряжений, в основе которых лежат их стандартные потенциалы,
этот ряд соответствует окислительно-восстановительном ряду металлов.
Запомните:
стандартный потенциал активных металлов, растворимых в кислотах, - негативный,
стандартный потенциал неактивных металлов, нерастворимых в кислотах, - положительный.
Стандартные
потенциалы двух окислительно-восстановительных пар позволяют рассчитать напряжение между
соответствующими напівелементами так называемого гальванического элемента. При этом
необходимо наличие стандартных условий, т.е. концентрация растворенных ионов
должна составлять с = 1 моль/л.
Пример.
Элемент Даниэля состоит из медного и цинкового электродов, погруженных
соответственно в раствор купрум(II) сульфата и цинка сульфата. Напряжение между
электродами составляет
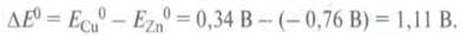
При
этом цинковый электрод является отрицательным электродом, поскольку отдает электроны меди:
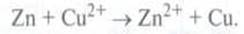
Внимание:
в гальваническом элементе электроны переходят от окислительно-восстановительной пары с более
отрицательным потенциалом к окислительно-восстановительной пары с более положительным потенциалом.