Часть И. ОБЩАЯ
ХИМИЯ
Раздел 7.
ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦІЇ.ЕЛЕКТРОЛІЗ
§
7.5. Классификация окислительно-восстановительных реакций
Обычно различают три типа
окислительно-восстановительных реакций: межмолекулярные, внутримолекулярные и реакции
диспропорціонування.
К межмолекулярных относятся реакции,
в которых окислитель и восстановитель входят в состав разных веществ. Рассмотренные в §7.3
и
7.4 реакции принадлежат к этому типу. Сюда также следует отнести и реакции между
различными веществами, в которых атомы одного и того же элемента имеют разные
степени окисления:
-2
+4
0
2H2S
+ H2SO3
= 3S
+ ЗН2О;
-1
+5
0
5НСl + НСlO3 = 5Сl2 + ЗН2О.
К
внутримолекулярных относятся такие реакции, в которых окислитель и восстановитель
входят в состав одной и той же ре човини. В этом случае атом с большим
положительным степенью окисления окисляет атом с меньшей степенью окисления. Такими
реакциями являются реакции термического разложения. Например:
+5
-2 +3
0
2NaNO3 = 2NaNO2 + О2;
+5
-2 -1
0
2КСlO2 = 2КСl + 3О2;
-С
+6 0
+3
(NH4)2Cr2O7 = N2+ Cr2O3, + 4Н2О.
Сюда также следует отнести и расписание
веществ, в которых атомы одного и того же элемента имеют разные степени
окисления:
-3
+3
0
NH4NO2
= N2
+ 2Н2O;
-С
+5
+1
NH4NO3 = N2O + 2Н2O.
Ход реакций диспропорціонування1
сопровождается одновременным увеличением и уменьшением степени окисления атомов одного
и того же элемента. При этом исходное вещество образует соединения, одна из которых
содержит атомы с высшим, а вторая - с более низкой степенью окисления. Очевидно, эти
реакции возможны для веществ, содержащих атомы с промежуточными степенями окисления.
Примером может быть превращение манганату калия К2МnО4, в котором марганец имеет
промежуточный степень окисления +6 (в примере между +7 и +4). Раствор этой соли имеет
красивый темно-зеленый цвет (цвет иона МnО2-4), однако
цвет раствора превращается в бурый. Это выпадает осадок МnO-4 и образуется ион МnO-4. Происходит реакция:
+6
+7 +4
3K2MnO4 + 2Н2O = 2КМnO4
+ МnО2
+ 4КOН;
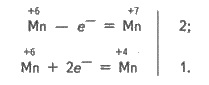
1
Диспропорция - отсутствие пропорциональности, несоизмеримость.
К реакциям диспропорціонування
относятся и такие реакции, которые часто встречаются:
+3
+5
+2
3HNO2 = HNO3 + 2NO + Н2O;
0
+1
- 1
Сl2 + Н2О -> HClO + НСl.
Ранее реакции диспропорціонування
называли реакциями самоокиснення - самовосстановления, теперь это название почти не
применяется.