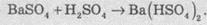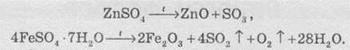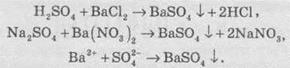ЧАСТЬ И
ОБЩАЯ ХИМИЯ
ХИМИЯ ЭЛЕМЕНТОВ
ОКСИГЕН. СУЛЬФУР
Сульфаты
Соли
серной кислоты, сульфаты, обычно представляют собой кристаллические вещества,
хорошо растворимы в воде (кроме PbSO4 и
BaSO4). Безводные сульфаты бесцветны, но некоторые
их соединения с водой (кристаллогидраты) имеют цвет: NiSO4 ∙ 7Н2O - интенсивно зеленый, FeSO4 ∙ 7Н2O - бледно-зеленый, а CuSO4 ∙
5Н2O
- синий. Кристаллогидраты сульфатов металлов называют купоросами.
Обычно
сульфаты добывают путем воздействия на карбонаты или гідрогенкарбонати металлов сульфатной
кислотой:

При
прокаливании сульфатов щелочных и щелочноземельных металлов до высоких температур
расписания соединения не происходит вплоть до плавления (около 2000 °С). При
нагревании сульфатов менее активных металлов происходит расписание на оксиды:
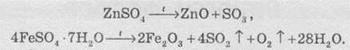
Сульфаты
металлов, находящиеся в электрохимическом ряду потенциалов правее водорода, разлагаются
на металл, сульфур оксид и кислород:
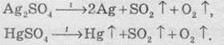
Кристаллогидраты
двойных сульфатов, которые содержат одновалентний и трехвалентный катион, имеют
название галуны. Например: K2SO4 ∙ Al2(SO4)3 ∙
24Н2O
- алюмокалієві галуны, K2SO4 ∙ Cr2(SO4)3 ∙
24Н2O
- хромокалієві галуны, (NH4)2SO4 ∙ Fe2(SO4)с ∙
24Н2O
- залізоамонійні галуны. Квасцы используют как дубильный средство в кожаном
производстве, при изготовлении бумаги, в фотографии, в медицине.
Применение
сульфатов в промышленности
|
Название
соединения
|
Формула соединения
|
Сфера
применение
|
|
Калий сульфат
|
K2SO4
|
Удобрение, производство квасцов
|
|
Натрий сульфат
|
Na2SO4
|
В целлюлозно-бумажной, мыловаренной
промышленности и при производстве стекла
|
|
Аммоний сульфат
|
(NH4)2SO4
|
Удобрение
|
|
Медный купорос
|
CuSO4 ∙ 5H2O
|
В сельском хозяйстве, в фотографии,
для травления металлов
|
|
Барий сульфат
|
BaSO4
|
В медицине
|
|
Сульфаты кальция - гипс и алебастр
|
CaSO4 ∙ 2H2O тa 2CaSO4 ∙ H2O
|
В строительстве
|
Сульфаты
используют почти во всех отраслях промышленности.
Качественная
реакция на сульфат-ион
В
аналитической химии используют реакцию взаимодействия хлорида или нитрата Бария с
образованием барий сульфата. При этом образуется белый мелкокристаллический осадок,
который не растворяется в кислотах и щелочах:
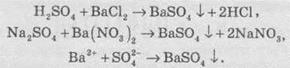
Полученный
осадок растворяется только в концентрированной сульфатной кислоте: