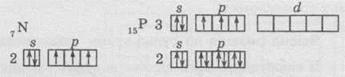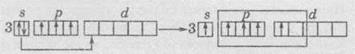|
Элементы
V группы главной подгруппы (Азот N, Фосфор
Р, Мышьяк As, Стибій
Sb и Висмут Ви)
называют также пніктогенами.
Нитроген
проявляет валентность, равную III, за счет образования связей с тремя
неспареними электронами p-подуровня:
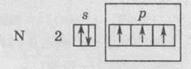
Валентность
IV проявляется за счет образования связи с участием электронной пары атома
Азота и свободной орбитали другого атома. При этом образуется обычный
ковалентная связь. Такой механизм называют
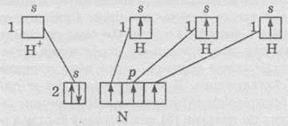
донорно-акцепторным механизмом образования ковалентной связи. Рассмотрим
образование такой связи на примере образования иона аммония NH4+:
Следовательно,
Азот может образовывать 3 ковалентные связи по обменному механизму и 1
связь по донорно-акцепторным механизмом. Общее количество возможных связей
равен 4, но максимальная степень окисления Азота равна +5. Пятивалентный
состояние Фосфора реализуется следующим образом:
Нитроген
может проявлять любую степень окисления от -3 до +5. Фосфор
гораздо легче образует соединения с положительной степенью окисления, чем с
отрицательным. Распространенность химических элементов
Азота и Фосфора Нитроген
- это довольно распространенный элемент в природе. На его долю приходится около 0,02%
массы Земли. Атомы Азота образуют простое вещество N2, которая в большом количестве содержится в атмосфере нашей планеты:
75,6% по массе, или 78,1% по объему. Азот входит в состав некоторых
минералов, например таких, как индийская селитра KNВ3 и чилийская селитра NaNВ3. Залежи натриевой соли тянутся на три
тысячи километров вдоль побережья Чили, отсюда происходит и название этого
минерала. Азот - это жизненно важный элемент. Он входит в состав белков,
нуклеиновых кислот, АТФ и многих других важных соединений. Организм человека
примерно на 2% состоит из Азота. Азот в больших количествах обнаружен
на 4 планетах Солнечной системы. Фосфор
является более распространенным элементом на Земле, чем азот. Содержание Фосфора в нашей
планете равна 0,088% по массе. Фосфор образует некоторые важные минералы, такие
как фторапатит Са5(РО4)
|
|