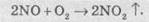ЧАСТЬ И
ОБЩАЯ ХИМИЯ
ХИМИЯ ЭЛЕМЕНТОВ
ОКСИГЕН. СУЛЬФУР
Сульфатная
кислота
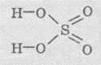
Структурная формула серной кислоты
имеет такой вид:
Физические
свойства серной кислоты
Сульфатная
кислота - это бесцветная, тяжелая, маслянистая жидкость, которая замерзает при температуре
+10 °С, а кипит при температуре +296 °С (кипит 98,3 % раствор, а избыток
серной кислоты разлагается на сульфатный ангидрид и воду). Плотность
серной кислоты при +20 °С равна 1,84 г/см3. 100% сульфатная
кислота почти не проводит электрический
ток. 95%-й раствор серной кислоты кристаллизуется при более низкой
температуре: -20 °С.
Эта
соединение очень гигроскопична, т.е. способна поглощать влагу из окружающей
среды. При этом выделяется большое количество тепловой энергии. Если
долить воду до серной кислоты, может выделиться столько энергии, что кислота
закипит и начнет разбрызгиваться по сторонам, поэтому для того, чтобы развести
концентрированную сульфатную кислоту, кислоту следует добавлять небольшими порциями к
воды.
Сульфатная
кислота способна растворять около 65% сульфатного ангидрида SO3. При этом образуется олеум.
Химические
свойства серной кислоты
Сульфатная
кислота является очень сильным окисником. В разбавленных растворах окисление проходит по
счет иона
Водорода, а в концентрированных растворах - за счет атома Серы(VИ).
Кислотные свойства серной кислоты
Сульфатная
кислота - это одна из самых сильных кислот. В разбавленных растворах она представляет собой
двухосновную кислоту, которая подвергается диссоциации по схеме:
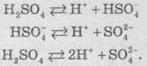
Сульфатная
кислота, так же, как и сульфитная, образует два ряда солей. К ним относятся
сульфаты (например, BaSO4 -
барий сульфат) и гідрогенсульфати (NaHSO4 -
натрий гідрогенсульфат). Сульфатная кислота энергично реагирует с разными основами
и основными оксидами, при этом образуются сульфаты:
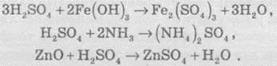
Реагирует
она и с металлами, которые передвигают в ряду стандартных электродных потенциалов
до водорода:
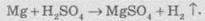
А
вот с железом концентрированная сульфатная кислота (≥ 75%) не реагирует, поэтому ее обычно
перевозят в стальных бочках и цистернах. Сульфатная кислота не реагирует также и
со свинцом, поскольку поверхность металла покрывается прочной пленкой нерастворимого
свинец(II) сульфата PbSO4, и
на этом процесс останавливается.
Окислительные свойства серной кислоты
В
концентрированных растворах при нагревании сульфатная кислота реагирует со многими
металлами, даже с некоторыми из тех, которые находятся в электрохимическом ряду
напряжений правее водорода:
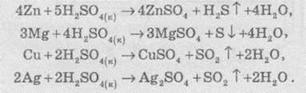
Продукты
восстановление серной кислоты, записанные в этих реакциях, не являются единственными. В общем,
во всех этих реакциях образуется смесь H2S, S, SO2, состав которой зависит от многих условий (концентрации кислоты,
температуры смеси, площади поверхности металла и т.д.), но записанный продукт у них есть
преобладающим.
При
нагревании концентрированная сульфатная кислота хорошо реагирует со многими неметаллами:
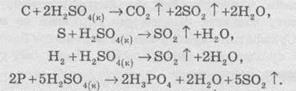
Сульфатная
кислота окисляет много сложных соединений:
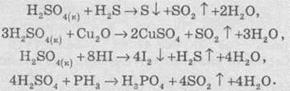
От
большинства органических соединений она отщепляет молекулы воды, что приводит к
обугливание соединения. Например, если на бумагу поместить каплю серной
кислоты, то через несколько секунд на месте этой капли образуется черное пятно,
которая состоит из углерода:
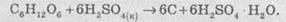
Значение
серной кислоты в народном хозяйстве
Сульфатная
кислота - важнейший продукт химической промышленности. Мировое производство
серной кислоты за год составляет сотни миллионов тонн.
Сульфатную
кислоту используют для производства различных летучих кислот, например, соляной,
уксусной, ортофосфатной, азотной и других, а также для производства азотных и
фосфатных удобрений (суперфосфата, аммоний фосфата и др.). Сульфатная кислота
необходима в производстве пластмасс, бумаги,
строительных материалов, тканей, лакокрасочных изделий и моющих средств. Ее
применяют для очистки нефти, нефтепродуктов и продуктов коксохимического
производства (бензену и толуола) от вредных примесей. Для производства эфиров,
ангидридов органических кислот и различных сульфопохідних также необходима сульфатная
кислота. В металлургической промышленности ее применяют для очистки поверхности
металлов перед нанесением покрытия. Раствор сульфатной кислоты используют как
электролит в кислотных аккумуляторах.
Сульфатная
кислота незаменима в хозяйстве.
Производство
серной кислоты
Сульфатную
кислоту добывают двумя различными методами: контактным и нитрозным. Независимо от
метода добывания, всегда присутствуют три основных этапа:
- добывания SO2;
- окисления SO2 в SO3;
- добывание серной кислоты.
Сульфитный
ангидрид SO2 обычно
добывают обжигом пирита (FeS2) как
побочный продукт при выплавке железа. Вместо пирита используют также некоторые
другие сульфиды (CdS, ZnS) или сероводород, выделенный из природного газа и нефти или
полученный при коксовании угля. Иногда используют простую вещество серу.
Контактный метод получения серной
кислоты
Перед
обжигом пирит измельчают для ускорения горения. Для увеличения выхода
сульфитного ангидрида в печь для обжига пирита дополнительно подают избыток кислорода.
Проходит такая реакция:
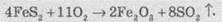
Схема
промышленной установки для производства серной кислоты контактным методом
изображена на рисунке:
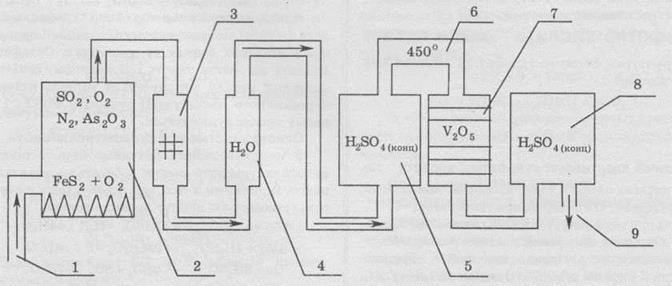
Процесс
работы этой установки заключается вот в чем. В печи (2) происходит сжигание
пирита. Кислород для горения подают через трубу (1). Поскольку в естественном
минерале пирита содержится около 20% примесей, то после обжига, конечно же, в
газах также будут примеси. Одной из таких примесей является арсен(III) оксид. Эта самая
по себе опасна для окружающей среды вещество является каталитической
ядом, то есть она нарушает работу катализатора. Для удаления этой вредоносной
примеси газовую смесь пропускают через специальные электрические фильтры (3) и
промывную башню с водой (4). После промывки водой смесь становится влажной, и, ради
удаление примесей воды, смесь пропускают через колонку с концентрированной
серной кислотой (5), которая эффективно поглощает влагу. Далее газовую смесь
нагревают в теплообменнике (6) до температуры 450°, и смесь попадает в контактный
аппарат (7), в котором находится катализатор V2O5 (в
роли катализатора иногда используют также ванадил сульфат VOSO4, платину или серебро). После этого
образован сульфур триоксид растворяют в концентрированной сульфатной кислоте (8),
вследствие чего образуется олеум, которым заполняют цистерны с помощью вывода
готового продукта (9).
Нітрозний
метод добывания серной кислоты
Около
20% серной кислоты, которую производят в мире, добывают нитрозным, или башенным,
методом. В этом методе окисления SO2 в
SO3 осуществляется азот диоксидом NO2:
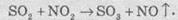
Нитроген
диоксид в этом методе регенерируется с помощью кислорода воздуха и снова вступает
в реакцию окисления сульфур(ИV)
оксида: