ОКИСЛЕНИЯ
И ВОССТАНОВЛЕНИЕ
1. Окислительно-восстановительные реакции
Окислительно-восстановительная
реакция состоит из двух напівреакцій: напівреакції окисления и напівреакції
восстановление. Окисление - это отдача электронов, восстановление - получение
электронов.
Пример.
При сгорании магния атомы Магния окисляются, а молекулы кислорода восстанавливаются.
При этом каждый атом Магния отдает два электрона каждому атому Кислорода.

1.1. Равновесие в окислительно-восстановительных
реакциях
На
отличие от приведенных выше определений «окисление» и «восстановление» возможны другие
определение этих понятий, например, для реакций без участия кислорода.

Пример.
Если поместить железный гвоздь в раствор купрум(II) сульфата, то через короткое
промежуток времени он покроется слоем металлической меди. При этом каждый атом Железа
отдаст по два электрона каждому иону Купруму.

Частица,
которая в окислительно-восстановительной реакции отдает электроны, является донором электронов.
Частица, получает электроны, является акцептор электронов.
Донор
электронов восстанавливает реагент и поэтому его называют восстановителем. Акцептор
электронов окисляющий реагент и поэтому его называют окисником. Следовательно,
окислительно-восстановительная реакция всегда проходит с участием восстановителя и окисника.
Которая
частичка в ходе окислительно-восстановительной реакции будет восстановителем или окисником,
зависит от того, какой из этих реагентов имеет большую склонность отдавать или
получать электроны (окислительно-восстановительный ряд).
Пример.
Если медный лист опустить в аргентум нитрат, то он покроется слоем
металлического серебра. В этом случае медь имеет большую склонность к отдаче
электронов и является, таким образом, восстановителем, а ионы Аргентуму - окисником:
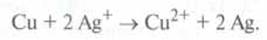
В
окислительно-восстановительной реакции восстановитель превращается в окислитель, а окислитель на
восстановитель. Обе стороны отражают равновесие окислительно-восстановительной реакции.
♦ Окислительно-восстановительная реакция сопровождается
переносом электронов.
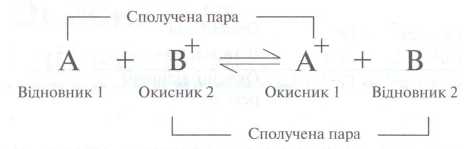
♦ Частицы, которые объединяются друг с другом в
результате отдачи или получения электронов, образуют сопряженную
окислительно-восстановительную пару.
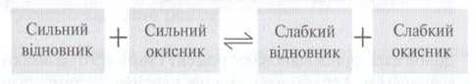
Запомните:
равновесие в окислительно-восстановительной реакции всегда смещена в сторону более слабого восстановителя и
окисника.
Внимание:
определение понятия «окислительно-восстановительная реакция» исходит из того же принципа,
что и определение понятия кислотно-основная реакция, по Бренстедом.
Окислительно-восстановительная реакция - это перенос электронов, кислотно-основная реакция -
перенос протонов.