КИСЛОТЫ
И ОСНОВЫ
3. Нейтрализация
3.2. Титрование кислот и оснований
Проведение титрования
Для
определение концентрации кислоты или щелочи нужно такое принадлежностей:
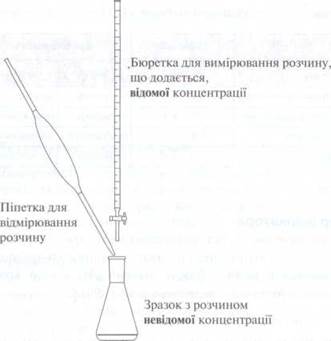
♦ пипетка для отмеривания определенного объема
кислоты или основания неизвестной концентрации;
♦ бюретка для измерения раствора известной
концентрации;
♦ Колба Ерленмейера (с образцом) для размещения
отмеренного объема раствора, что определяется, неизвестной концентрации.
После
добавление соответствующего индикатора для титрования в испытуемый раствор с
бюретки каплями добавляют раствор известной концентрации, пока не состоится нужна
изменение окраски. Расходы раствора измеряют и записывают.
Пример.
Етанову кислоту с неизвестной концентрацией титруют 0,1 М раствором едкого натра
в присутствии фенолфталеина в качестве индикатора.
Известны
величины:
• концентрация раствора едкого натра (щелочи): сЛ
= 0,1 моль/л;
• использованный объем раствора едкого натра: VЛ = 25 мл;
• отмеренный объем етанової кислоты: VK = 10 мл.
Расчет
концентрации ск:
• потрачена химическое количество едкого натра в
растворе:
nЛ = сл
∙
VЛ
= 0,1 моль/л ∙
25 ∙
10-3 л = 2,5 ∙
10-3 моль.
Поскольку
в растворе едкий натр продисоціював полностью, то это химическое количество соответствует
используемой химической количества гидроксид-ионов. Они в свою очередь вступают в
реакцию с таким же химическим количеством ионов гідроксонію, которые образуются из
такой же химической количества етанової кислоты. Поэтому:
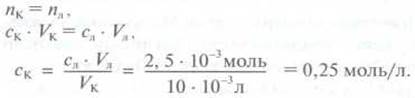
Используя
молярну массу етанової кислоты, можно рассчитать также массовую концентрацию -
титр (Т):
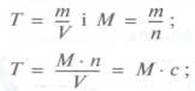
М
(етанова кислота) = 60 г/моль;
Т
= 60 г/моль ∙
0,25 моль/л = 15 г/л.