СТРОЕНИЕ АТОМА
5. Модель
строения электронных оболочек атомов
Основные
предположения теории Бора можно перенести в качественном отношении на простые системы
с несколькими валентными электронами, например, такие как атомы щелочных металлов.
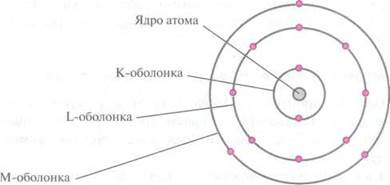
♦ Электроны располагаются вокруг ядра на
оболочках (слоях).
♦ Всего в атомах различают до семи оболочек
(слоев).
♦ Каждая оболочка является определенным уровнем энергии и может
содержать определенное число электронов.
Запомните:
общая формула, определяющая максимальное число электронов в оболочке, - 2n2, где квантовое
число n
является номером оболочки.
Максимальное
число электронов заполненных электронных оболочек
|
Номер
оболочки = квантовое число
|
Обозначения
оболочки
|
Максимальное
число электронов
|
|
1
|
К
|
2
|
|
2
|
L
|
8
|
|
3
|
М
|
18
|
|
4
|
N
|
32
|
|
5
|
В
|
50
|
|
6
|
Г
|
72
|
|
7
|
Q
|
98
|
Каждый
атом элемента имеет определенное число электронных оболочек (слоев):
♦ внешнюю оболочку называют оболочкой валентных
электронов;
♦ электроны, которые находятся на оболочке
валентных электронов, называют валентными электронами.
Прибор.
Модель атома Алюминия
Валентные
электроны отвечают за химические свойства элементов, а также за химический
связь между атомами.
Достижения модели строения электронных оболочек атомов
♦ определены относительные размеры атомов
различных элементов;
♦ объяснено разную энергию ионизации атомов;
♦ обоснованы и предусмотрено различную реакционную
способность элементов;
♦ обоснована способность образовывать связь между
атомами элементов (ионная связь, ковалентная связь).