Часть 2 МОЛЕКУЛЯРНАЯ ФИЗИКА И ТЕРМОДИНАМИКА
Раздел 6 СТРОЕНИЕ И СВОЙСТВА ВЕЩЕСТВА В КОНДЕНСИРОВАННОМ СОСТОЯНИИ
6.1. Строение и свойства кристаллов
Существенной особенностью кристаллического
тела является упорядоченность в размещении частиц, из которых оно построено: атомов,
молекул, ионов и т.д. Удобным способом описания этого размещения частиц являются пространственные
решетки.
Вследствие упорядоченного размещения
частиц кристаллы приобретают свойства, которых не имеют некристаллические тела.
Одним из таких свойств является плоскогранність и постоянство углов между гранями
монокристаллов. Эта особенность кристаллических тел часто сразу бросается в глаза, потому
внешнюю форму кристаллов было изучено значительно раньше, чем экспериментально
исследованы их внутреннее строение. Если мы говорим о какой-нибудь кристалл, то
у нас возникает образ тела, которая имеет определенную правильную форму, а не представление о
упорядоченность в размещении частиц, хотя последнее является основным свойством кристалла.
Важнейшими свойствами кристалла, обусловленными закономерным распределением
частиц в нем, является анизотропия, симметрия в распределении направлений с одинаковыми
физическими свойствами, однородность.
В XIX в. накоплен большой
экспериментальный материал по изучению кристаллов. Было выдано одинадцятитомну
труд русского ученого М. И. Кокшарова (1818-1892) «Материалы по минералогии
России». Однако собранный на то время материал еще не имел теоретического обоснования
и обобщения. Попытки некоторых ученых встречали упрямую противодействие со стороны
немецкой формальной школы, представители которой отрицали реальное существование
атомов. Есть. С. Федоров, в отличие от формальной школы немецких
кристалографів, создал теорию кристаллов, положив в основу ее единственный
геометрический базис. В 1885 г. вышла в свет первая монография Является. С. Федорова
«Начала учения о фигурах». С этого момента в истории кристаллографии
начинается новый период.
Есть. С. Федоров показал, что существует
четыре типа пространственных фигур (многогранников), заполняющих пространство. Первые
три типа федорівських решеток - кубические, четвертая - гексагональная. Следовательно, по
Федоровым, существуют два основных типа пространственных решеток: кубические и гексагональные. Ему принадлежат также открытие 32
совокупностей элементов симметрии для кристаллических тел, 230 способов размещения
частиц в кристаллах, открытие кристалохімічного анализа и создания
специальной аппаратуры и методов исследования кристаллов.
Большое научное значение имеет
применение рентгеновского излучения для исследования микроструктуры
кристаллов. Разрабатывая теорию рассеяния рентгеновского излучения кристаллами,
Г. В. Вульф в России и Л. Брэгг в Англии вывели важное уравнение, которое называют
формуле Вульфа - Брэгга:

где
d - расстояние между параллельными
атомными плоскостями; θ - угол между направлением падающего
луча и отражающей атомной плоскостью кристалла; λ - длина волны рентгеновского
излучения; n = 1, 2, 3,...________
Формула Вульфа - Брэгга характеризует
особенность отражения рентгеновского излучения кристаллом, которая является
следствием интерпретации лучей, рассеянного атомами, расположенными в узлах пространственной
решетки.
Для определения строения кристаллов
помощью рентгеновского излучения используют рентгеновский анализ,
предназначен для расшифровки рентгенограмм. Для этого широко используют
метод проб и ошибок, который заключается в построении такой модели кристалла, когда
теоретически вычисленная рентгеноструктурна картина совпадает с экспериментальной.
В 1946 г. на основе идеи плотного
упаковка молекул В. И. Китайгородский разработал геометрический метод
структурного анализа, что позволяет определить ориентацию молекул в кристалле. Чтобы
воспользоваться этим методом, надо знать только элементарную ячейку и симметрию
кристалла.
В разработке методов
рентгенографического изучения структуры большая роль принадлежит М. В. Белову.
В последнее время широко используются електронографічний и нейтронографічний
методы изучения строения кристаллов.
Одним из результатов упорядоченного
размещение частиц в кристаллических телах является неодинаковость многих физических свойств
монокристаллов в различных направлениях. Так, от направления зависит теплопроводность,
электрическое сопротивление, коэффициент теплового расширения, прочность на разрыв, показатель
преломления света, диэлектрическая проницаемость и т.д. Однако есть и такие кристаллы, для
которых не все перечисленные свойства зависят от направления. Например, в
кристаллах, элементарная ячейка которых имеет форму куба, не зависят от направления
такие свойства, как электрическое сопротивление, коэффициент теплопроводности, показатель
преломление света и некоторые другие. Есть и такие свойства, что никогда не зависят от
направления, хоть бы какая была строение кристалла, например плотность.
Зависимость физических свойств от
направления называют анизотропией. Тела, для которых какое-то свойство зависит от
направления, называют анизотропными. Тела, физические свойства которых от направления не зависят, называют ізотропними. Монокристаллы есть
анизотропными, по крайней мере относительно некоторых физических свойств. Поликристаллы
вообще изотропные, но могут стать анизотропными под влиянием внешних воздействий
(тепловых, механических и т.д.). Внешними действиями можно сделать анизотропными
даже некристаллические тела.
Итак, хоть анизотропия - свойство
кристалла, которая возникает вследствие упорядоченного размещения частиц, она не является
качественной особенностью кристалла. И в некристаллических телах анизотропия может возникнуть,
если в них вследствие воздействия внешних факторов образуется определенный степень
упорядоченности в размещении молекул.
В начале XX в. окончательно сложились
представление о роли сил притяжения и отталкивания в кристалле. Если на кристалл
не действуют внешние силы, то размещение частиц соответствует равенству сил
притяжения и отталкивания, действующих на каждую частицу со всех сторон. В случае
действия на кристаллическое тело внешних сил, которые пытаются растянуть его,
расстояние между частицами увеличивается, а силы притяжения преобладают над силами
отталкивания и после прекращения действия внешней силы возвращают частицы в
начальное положение. Наоборот, при попытке сжать тело, оно сопротивляется,
поскольку преобладают силы отталкивания.
Согласно современным представлениям существует
четыре типы связи в твердых телах: ионная, ковалентная, металлическая и
вандерваальсовий. В соответствии с характером сил связи все кристаллы делятся
на четыре группы. К первой группе относятся ионные кристаллы. Типичным примером ионных
кристаллов являются кристаллы NаСl, состоящие из почережно расположенных положительных ионов
Nа и отрицательных ионов Сl (рис. 6.1). Ионные кристаллы конечно
не проводят электрического тока, поскольку в них электроны прочно удерживаются на
орбитах отдельных ионов. Однако при нагревании ионные кристаллы становятся проводниками
с ионной проводимостью.
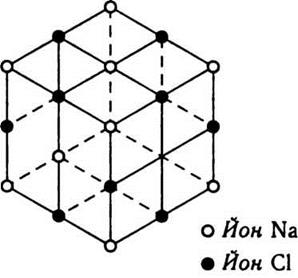
Рис. 6.1
Ко второй группе относятся атомные
кристаллы. Они построены из атомов, которые связаны друг с другом ковалентной
связью, то есть таким, который осуществляется вследствие того, что в двух или нескольких
атомов есть общие электроны. До атомных кристаллов относятся, например, кристаллы
алмаза, серы. На рис. 6.2 показано строение
кристаллической решетки алмаза. Атомные кристаллы не проводят электрического тока не
только при средних, а при высоких температурах и даже в расплавленном состоянии.
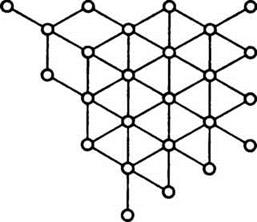
Рис. 6.2
В случае ковалентной связи силы
связи имеют направленный характер. Так, у атомов алмаза связи осуществляются в
четырех направлениях, которые образуют один
с одним углы 109° 30'. Второй особенностью ковалентной
связи является то, что силы действуют как в направлении прямой, соединяющей частицы, так и в
направлении, перпендикулярном к ней.
Особую группу кристаллов составляют
металлы. С точки зрения межатомных связей металлы и сплавы металлов можно рассматривать
как совокупность положительных ионов, которые содержатся в среде свободных электронов,
хаотично двигаются. Природа металлической связи существенно отличается от ионного
связи, но общим для них является независимость сил связи от взаимного
ориентации частиц. Металлы отличаются от других кристаллических веществ доброй
тепло - и электропроводностью, оптической непрозрачностью и высокой отражающей
способностью (блеском).
Еще одну группу кристаллов составляют
молекулярные кристаллы с вандерваальсовим связью, обусловленный электрической
взаимодействием между молекулярными диполями. Примерами могут быть кристаллы СO2, O2, N2 в твердом состоянии. Низкая точка
плавления, большие сжимаемость и коэффициент теплового расширения этих тел
свидетельствуют о том, что этот тип связи очень слабый. В некоторых твердых телах осуществляется
не один, а два и более типов связи. Так, в кристаллах графита есть три типа
связи: ковалентная и металлическая в пределах одного плоского слоя и
вандерваальсовий между слоями. Все тела, в том числе и металлы расширяются при
нагревании. Опыт показывает, что только увеличением амплитуды колебаний атомов
тепловое расширение тел, объяснить нельзя. Надо, кроме того, принять во внимание
характер сил, действующих между атомами и вызывают колебания атомов вокруг
положение равновесия. Если бы все эти силы были гармоничными, т.е. пропорциональными
смещение атома от положения равновесия, то теплового расширения не было бы.
На самом деле эти силы ангармонических, что и обусловливает тепловое расширение.
Кривую потенциальной энергии двух
атомов, которые взаимодействуют, изображен на рис. 6.3. Положению равновесия, или центра
колебаний, соответствует минимум потенциальной энергии. Это положение характеризуется
расстоянием r0 между атомами и соответствует равенству
сил притяжения и сил отталкивания между атомами. На расстоянии r r0
преобладает сила отталкивания, а на расстоянии r > r0 - сила притяжения. При малом
смещении атома из положения равновесия сила, которая возвращает его в положение
равновесия, прямо пропорциональна смещению. Однако при значительном смещении
пропорциональности между смещением и обратной силой нарушается.
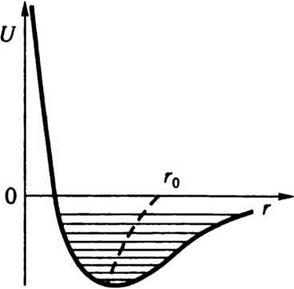
Рис. 6.3
Если пересечь кривую потенциальной
энергии горизонтальными прямыми, то полная энергия атома, что колеблется,
будет определяться расстоянием соответствующей прямой от оси абсцисс. Точка, которая разделяет
пополам каждую из этих прямых, определяет соответствующее положение равновесия. Принимая во внимание, что на рис. 6.3 полная энергия растет
снизу вверх, и сравнивая положения точек равновесия, или центров колебаний, при
различных энергиях, видим, что при увеличении энергии атома, что колеблется,
положение центра колебаний смещается вправо. Следовательно, при нагревании расстояние между
центрами колебаний атомов должна возрастать, то есть тело должно расширяться, что мы и
наблюдаем в действительности. Вещество в твердом состоянии может быть как кристаллической,
так и аморфной. Примерами твердых аморфных тел является янтарь, стекло, различные пластмассы.
По своему молекулярному строению аморфные тела занимают промежуточное положение между
жидкостями и кристаллами. Твердые аморфные тела имеют строение, характеризующееся
наличием ближнего порядка в размещении частиц. Этим они подобны жидкостей и
отличаются от кристаллов, в которых кроме ближнего порядка является также далек
порядок. Твердые аморфные тела, как и жидкости, изотропные, т.е. их физические
свойства одинаковы во всех направлениях (если внешние воздействия не вызывают
анизотропии). В отличие от жидкостей, где ближний порядок меняется с изменением
температуры, в аморфных телах он сохраняется в достаточно широких пределах
температур.
Из жидкого состояния в твердое аморфное
состояние вещество переходит не при определенной температуре, а в некотором интервале
температур. Во время перехода вещества из жидкого состояния в аморфное, а также под
время обратного перехода из аморфного в жидкое все физические свойства - удельное
объем, удельная теплоемкость, диэлектрическая стала и т.д. - изменяются непрерывно,
в отличие от явления кристаллизации, когда эти свойства меняются
скачкообразно.
Особый научный интерес представляет
также жидкокристаллический (или мезоморфный) состояние вещества, что имеет структурные
свойства, которые являются промежуточными между свойствами твердого кристалла и жидкости.