КИСЛОТЫ
И ОСНОВЫ
3. Нейтрализация
При
смешивании равных объемов соляной кислоты и раствора едкого натра одинаковых
концентраций, образуется нейтральный раствор натрий хлорида, имеет показатель pH = 7. Таким образом, кислотные и щелочные
свойства исходных веществ нейтрализуются.
Нейтрализация
является реакцией взаимодействия ионов гідроксонію и гидроксид-ионов с образованием молекул
воды:
Н3О+
+ ОН- 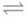 2 Н2О.
2 Н2О.
Внимание:
равновесие практически полностью смещено в сторону образования воды (автопротоліз воды).
Анион
кислоты (например, хлорид-ион в растворе соляной кислоты) и катион щелочи
(например, ион Натрия в растворе едкого натра) в процессе нейтрализации не
участвуют. Это утверждение верно для случая, когда и кислота, и щелочь
дисоційовані полностью.
3.1. Нейтрализация слабых кислот и оснований
Слабые
кислоты и основания при нейтрализации ведут себя иначе.
♦ Поскольку ионы гідроксонію и гидроксид-ионы
во время нейтрализации постоянно удаляются с протолітичної равновесия, то их
концентрация должна возобновляться в равном объеме за счет диссоциации
слабых электролитов.
♦ Раствор соли, образованный в результате
проведенной нейтрализации, не нейтрален, поскольку один из ионов (или оба ионы)
реагируют с молекулами воды, которая, согласно теории Бренстеда, может проявлять
свойства кислоты или основания.
Пример
1. В водном растворе етанової кислоты содержится небольшое количество ионов
гідроксонію. При нейтрализации с использованием раствора едкого натра эти ионы
удаляются из равновесия и поэтому пополняются за счет диссоциации молекул
етанової кислоты. После проведения нейтрализации образовавшийся раствор натрий
ацетата имеет щелочную среду, так как ацетат-ион вступает в реакцию с водой:

Пример
2. В водном растворе аммиака содержится небольшое количество гидроксид-ионов.
Во время нейтрализации с использованием соляной кислоты эти ионы удаляются из
равновесия и поэтому пополняются за счет протолізу молекул аммиака. Раствор
аммоний хлорида, образующийся в результате нейтрализации, имеет кислую среду,
поскольку ион аммония вступает в реакцию с водой:
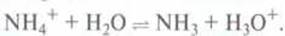
Изменения
значение pH раствора при добавлении кислоты или щелочи представлены в
виде кривой титрования.
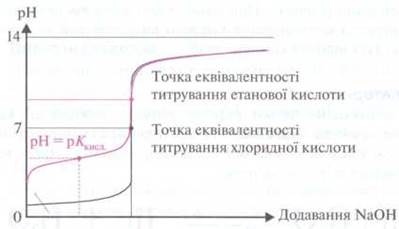
Запомните:
точкой эквивалентности называют точку на кривой титрования при отсутствии
избытка как кислоты, так и щелочи. При титровании слабой кислоты точка
эквивалентности на кривой титрования находится в щелочной области значений pH, при титровании слабого основания раствором
сильной кислоты точка эквивалентности находится в кислой области значений pH.
На
кривой титрования слабых кислот и оснований, кроме точки эквивалентности, есть еще
поворотная точка. В этом месте происходит превращение половины кислоты или
основы на соответствующую связанную основание или кислоту. Поскольку в этом случае
образуется буферный раствор в соотношении концентраций соль : кислота или
соль : основа, равном 1:1, то значение pH или
значение рОН, согласно буферного уравнения, соответствует значению рКкисл.
или значению рКосн. кислоты или основания.
Внимание:
кривые титрования багатоосновних кислот, молекулы которых могут диссоциировать
ступенчато, имеют соответственно больше точек эквивалентности.