КИСЛОТЫ
И ОСНОВЫ
2. Протолітична
равновесие
2.5. Буферные растворы
Действие буферов
Используя
константу равновесия процесса диссоциации кислоты, можно показать действие буфера:
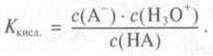
♦ Добавление кислоты, то есть увеличение с(Н3О+).
Для
сохранение равновесия добавлены ионы гідроксонію реагировать с соответствующими ионами
А-, образуя недисоційовану, практически не изменяя концентрацию
ионов гідроксонію.
♦ Добавление щелочи, т.е. увеличение с(ОН-).
Добавлены
гидроксид-ионы реагируют с частью ионов Н3О+, образуя
молекулы воды. Для сохранения равновесия часть НА диссоциирует на А- и
Н3О+, тем самым сохраняя неизменным значение
концентрации ионов гідроксонію.
Поскольку
концентрации НА и А- по сравнению с концентрациями Н3В очень
большие, то изменение концентрации Н3О+ при добавлении кислот
или щелочей практически незаметна.
Пример.
Если растворить 0,1 моль гидроген хлорида в 1 литре воды, то концентрация ионов
гідроксонію изменится с с(Н3О+) = 10-7 моль/л
на с(Н3О+) = 10-1 моль/л. Таким образом,
значение pH снизится с 7 до 1.
Если
ту самую порцию вещества гидроген хлорида растворить в 1 литре ацетатного буфера,
состоящий из, соответственно, 1 моль етанової кислоты и 1 моль натрий ацетата,
то добавлены ионы гідроксонію согласно уравнению
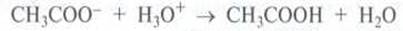
взаимодействуют с 0,1 моль ацетат-ионов,
образуя 0,1 моль етанової кислоты. В обеих составных частях буфера будут
такие новые концентрации:
с(соли)
= (1 - 0,1) моль/л = 0,9 моль/л;
с(кислоты)
= (1 + 0,1) моль/л =1,1 моль/л.
Отсюда
для показателя pH раствора:
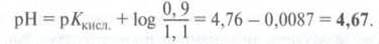
Показатель
pH буфера
составлял сначала 4,76, при добавлении гидроген хлорида практически не изменился.
Как
буфер может нейтрализовать изменение показателя pH, зависит от
соотношение концентраций соль : кислота или соль : основа. Чаще всего
используют отношение объемов растворов веществ 1:1 одинаковых концентраций.
Запомните:
буферные растворы применяют в тех случаях, когда показатель pH системы не должен существенно меняться
под влиянием внешних воздействий.