РАЗДЕЛ И. ОБЩАЯ ХИМИЯ
6. Смеси веществ. Растворы
Примеры решения типовых задач
Задача 1. В растворе, масса которого 400 г, содержится 25 г натрий хлорида. Вычислите массовую долю натрий хлорида (%) в растворе.
Дано:
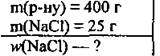
Решение
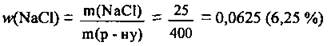
Ответ: w(NaCl) = 6,25 %.
Задача 2. Натрий гидроксид, масса которого 10 г, растворили в 120 мл воды. Вычислите массовую долю щелочи (%) в полученном растворе.
Дано:
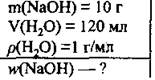
Решение
1. Рассчитаем массу воды по формуле 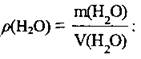
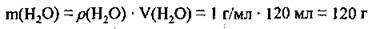
2. Вычислим массу раствора:
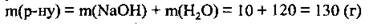
3. Вычислим массовую долю NaOH в полученном растворе:
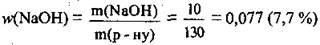
Ответ: w(NaOH) = 7,7 %.
Задача 3. Вычислите массу калий хлорида и объем воды, которые нужно использовать для приготовления 0,2 кг раствора с массовой долей соли 0,03.
Дано:
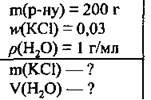
Решение
1. По формуле 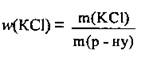 вычислим массу соли, которая должна быть в растворе:
вычислим массу соли, которая должна быть в растворе:
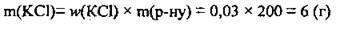
2. Вычислим массу воды в растворе.
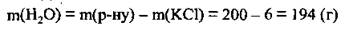
3. По формуле 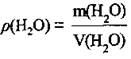 рассчитаем объем воды:
рассчитаем объем воды:
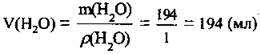
Ответ: m(КСl) = 6 г; V(H2O) = 194 мл.
Задача 4. Вычислите массовую долю хлороводорода (%) в растворе, который получили доливкой 50 мл воды до 200 мл соляной кислоты с массовой долей хлороводорода 20 %. Плотность этого раствора - 1,098 г/мл.
Дано:
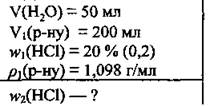
Решение
1. По формуле 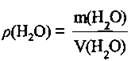 определим массу воды:
определим массу воды:
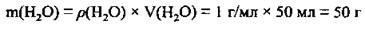
2. По формуле 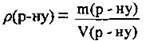 вычислим массу раствора хлороводорода (И):
вычислим массу раствора хлороводорода (И):
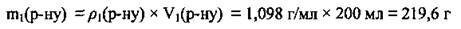
3. По формуле 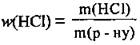 определим массу хлороводорода в растворе (И):
определим массу хлороводорода в растворе (И):
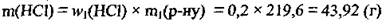
4. Вычислим массу воды:
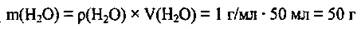
5. Найдем массу образовавшегося (после доливки воды) раствора (II):
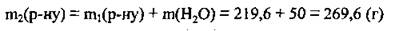
6. По формуле 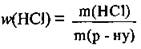 вычислим массовую долю хлороводорода в полученном растворе:
вычислим массовую долю хлороводорода в полученном растворе:
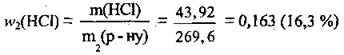
Ответ: w2(HCl) = 16,3 %.
Задача 5. При частичном испарении 300 г раствора калия хлорида с массовой долей соли 15% получили 140,6 г нового раствора. Вычислите массовую долю калий хлорида (%) в нем.
Дано:
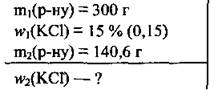
Решение
1. По формуле 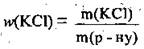 определим массу соли в исходном растворе:
определим массу соли в исходном растворе:
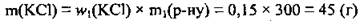
2. Во время испарения уменьшилась масса раствора за счет воды, которая испарялась; масса же соли осталась неизменной. По той же формуле вычисляем массовую долю соли в новом растворе:
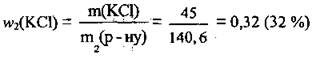
Ответ: w2(KCl) = 32 %.
Задача 6. В 0,5 л воды растворили 89,6 л хлороводорода (н. у.). Вычислите массовую долю хлороводорода (%) в полученной хлоридной кислоте.
Дано:
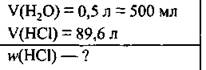
Решение
1. По формуле 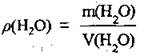 вычислим массу воды, которую использовали для приготовления раствора ρ(Н2O) = 1 г/мл:
вычислим массу воды, которую использовали для приготовления раствора ρ(Н2O) = 1 г/мл:
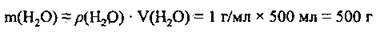
2. Определим массу хлороводорода. VM = 22,4 л/моль, М(НСl) = 36,5 г/моль:
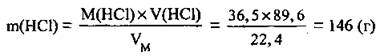
3. Вычисляем массу полученного раствора:
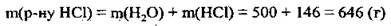
4. Находим массовую долю НСl в полученном растворе:
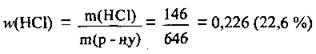
Ответ: w(HCl) = 22,6 %.
Задача 7. Вычислите массу феррум(II) сульфата гептагідрату, которую нужно использовать для приготовления 228 г раствора с массовой долей ферум(ІІ) сульфата 0,2.
Дано:

Решение
1. По формуле 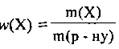 вычислим массу соли в растворе:
вычислим массу соли в растворе:
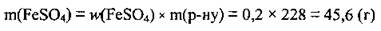
2. Рассчитаем количество вещества FeSO4. M(FeSO4) =152 г/моль:
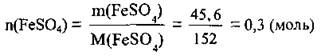
3. Вычислим количество вещества феррум(II) сульфата гептагідрату. Из химической формулы кристаллогидрата видно, что 1 моль содержит 1 моль ферум(ІІ) сульфата:
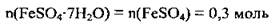
4. Вычислим массу кристаллогидрата количества вещества 0,3 моль. M(FeSO4 · 7H2O) = 278 г/моль:
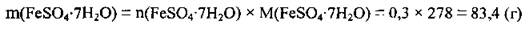
Ответ: m(FeSO4 · 7H2O) = 83,4 г.
Задача 8. В 120 г раствора купрум(II) сульфата с массовой долей соли 25 % растворили 6 г медного купороса. Вычислите массовую (%) долю купрум(II) сульфата В полученном растворе.
Дано:
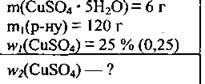
Решение
1. По формуле 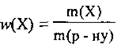 вычислим массу купрум(II) сульфата в начальном растворе:
вычислим массу купрум(II) сульфата в начальном растворе:
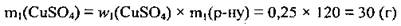
2. Найдем количество вещества медного купороса. M(CuS04 · 5Н2O) = 250 г/моль:
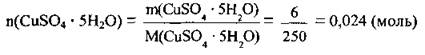
3. Определим количество вещества купрум(II) сульфата в составе медного купороса. Из формулы медного купороса CuSO4 · 5Н2O видно, что 1 моль кристаллогидрата содержит 1 моль CuSO4. Следовательно,
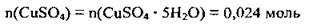
4. Вычислим массу 0,024 моль купрум(II) сульфата. M(CuSO4) = 160 г/моль:
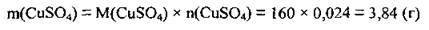
5. Рассчитаем массу полученного раствора:
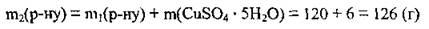
6. Вычислим массу купрум(II) сульфата в полученном растворе:
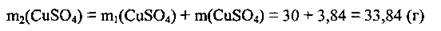
7. Определим массовую долю соли в полученном растворе:
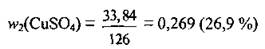
Ответ: w2(CuSO4) = 26,9 %.
Задача 9. Вычислите массу натрий сульфата в 400 мл раствора с молярною концентрацией соли 2 моль/л.
Дано:
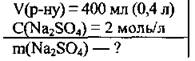
Решение
1. По формуле 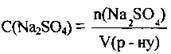 вычислим количество вещества соли в растворе:
вычислим количество вещества соли в растворе:
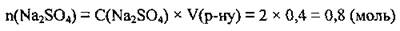
2. По формуле 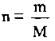 вычислим массу Na2SO4. M(Na2SO4) = 142 г/моль:
вычислим массу Na2SO4. M(Na2SO4) = 142 г/моль:
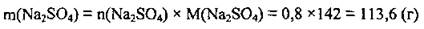
Ответ: m(Na2S04) = 113,6 г.
Задача 10. Вычислите молярну концентрацию щелочи в 800 мл раствора, который содержит 84 г калий гидроксида.
Дано:
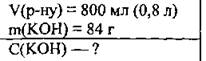
Решение
1. По формуле 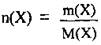 вычислим количество вещества щелочи в растворе. М(КОН) = 56 г/моль:
вычислим количество вещества щелочи в растворе. М(КОН) = 56 г/моль:
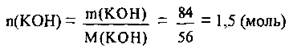
2. Вычислим молярну концентрацию щелочи в растворе:

Ответ: С(КОН) = 1,875 моль/л.
Задача 11. Насыщенный при 40 °С раствор, масса которого 80 г, содержит 10,4 г калий сульфата. Вычислите: 1) количество вещества воды в растворе; 2) массовую долю калий сульфата (%); 3) растворимость соли.
Дано:
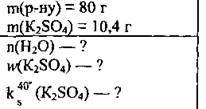
Решение
1. Вычисляем массу воды в растворе:
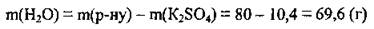
2. Найдем количество вещества воды. М(Н2O) = 18 г/моль:
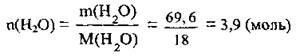
3. Вычислим массовую долю соли в растворе:
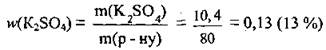
4. Определим растворимость соли. Составим пропорцию:
в 69,9 г Н2O растворяется 10,4 г K2SO4,
а в 100 г Н2O - х г K2SO4
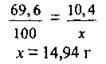
Ответ: 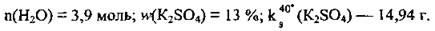
Задача 12. Вычислите объем раствора калий гидроксида с массовой долей щелочи 10 % (ρ = 1,08 г/мл), необходимый для полной нейтрализации 24,5 г ортофосфатной кислоты.
Дано:
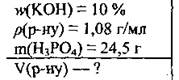
Решение
1. Рассчитаем количество вещества Н3РO4. М(Н3РO4) = 98 г/моль:

2. Напишем уравнение химической реакции:
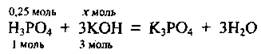
Из уравнения следует такая пропорция: 1 моль Н3РO4 соответствует 3 моль КОН, а 0,25 моль Н3РO4 - х моль КОН
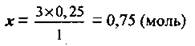
4. По формуле 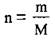 вычислим массу 0,75 моль КОН. М(КОН) = 56 г/моль:
вычислим массу 0,75 моль КОН. М(КОН) = 56 г/моль:
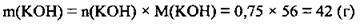
5. По формуле 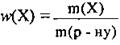 определим массу раствора калий гидроксида:
определим массу раствора калий гидроксида:
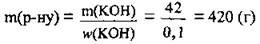
6. По формуле р(г-ну) 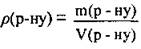 вычислим объем раствора КОН:
вычислим объем раствора КОН:
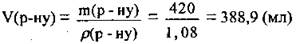
Ответ: V(р-ну) = 388,9 мл.
Задача 13. Растворимость магния сульфата при температуре 85 °С составляет 65 г на 100 г воды. Определите массу безводной соли, которую можно получить при выпаривании 340 г такого насыщенного раствора.
Дано:
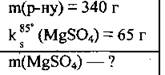
Решение
1. Растворимость магния сульфата при 85 °С составляет 65 г на 100 г воды. Итак, в каждых 100 г воды максимально может раствориться 65 г соли. Масса этого раствора составляет:
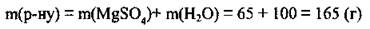
2. Составим пропорцию: 165 г раствора содержит 65 г MgSO4, а 340 г раствора - х г MgSO4.
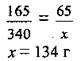
Ответ: m(MgSO4) = 134 г.