РАЗДЕЛ И. ОБЩАЯ ХИМИЯ
6. Смеси веществ. Растворы
6.4. Строение молекулы воды. Водородная связь между молекулами воды
В молекуле воды имеются две ковалентные полярные связи между атомом Кислорода и двумя атомами Водорода. За большой разницы электроотрицательности Кислорода (3,5) и Водорода (2,2) электронные облака смещены в сторону Кислорода, вследствие чего молекула воды представляет собой диполь.
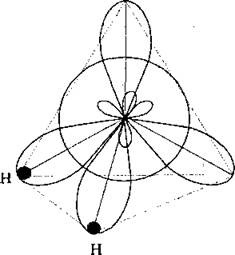
При образовании молекулы воды происходит sp3-гибридизация электронных орбиталей атома Кислорода. Две sp3-орбитали идут на образование связи с Гідрогеном. У атома Кислорода остается еще две sp3-орбитали, заполненные спаренными электронами.
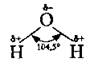
Через неравноценность состояний электронных облаков валентный угол связей Н-О несколько отличается от тетраедричного и составляет 109,5°, а 104,5°:
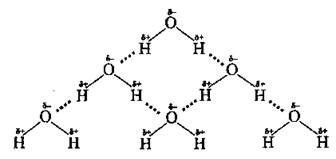
Между молекулами воды существуют водородные связи, благодаря которым молекулы соединяются между собой (в жидком и твердом состояниях), образуя так называемые кластеры и клатраты (ассоциаты), которые можно увидеть с помощью фазово-контрастного микроскопа. Сила водородной связи между молекулами воды в 20 раз меньше силу ковалентной связи Н-0 в самой молекуле. Схема водородных связей между молекулами воды: