РАЗДЕЛ И. ОБЩАЯ ХИМИЯ
6. Смеси веществ. Растворы
6.3. Растворы
Растворы - гомогенные (однородные) смеси из двух (или нескольких) веществ, относительные количества которых могут значительно варьироваться.
Любой раствор состоит из растворенного вещества (веществ) и растворителя, т.е. среды, в котором молекулы или ионы этого вещества равномерно распределены.
Растворитель - это компонент раствора, агрегатное состояние которого при образовании раствора не меняется. Если смешиваются твердое вещество с твердой, жидкость с жидкостью или газ с газом, растворителем считают тот компонент, количество которого больше. Иногда газы растворяются в твердых веществах, например, водород в металлах (платине, палладии).
По агрегатному состоянию различают твердые (металлические сплавы), газообразные (например, воздуха) и жидкие растворы. Чаще всего под словом «раствор» понимают жидкость.
На практике в основном мы имеем дело с водными растворами, то есть такими, в которых растворителем является вода. В таком случае воду считают растворителем и тогда, когда ее количество меньше количества растворенного в ней вещества: например, говорят о 70 %-й раствор спирта в воде, а не о 30 %-й раствор воды в спирте; о растворенные в воде кислоты (независимо от концентрации), а не о воду, растворенную в кислоте.
Растворимость вещества S (от лат. solvere - растворять) - это способность вещества растворяться в растворителе; определяется количеством вещества, которое может раствориться в определенном количестве растворителя, образовав при данной температуре насыщенный раствор.
Растворимость твердых и жидких веществ в воде с повышением температуры обычно существенно увеличивается, хотя встречаются и такие случаи, когда она возрастает в незначительной степени (NaCl, АlСl3) или даже уменьшается (Са(ОН)2, Na2SО4, Са(СН3СОО)2). Растворимость газов возрастает с повышением давления и уменьшается с повышением температуры.
Обычно полярные (ковалентные и йонни) соединения хорошо растворяются в полярных растворителях, а неполярные вещества - в неполярных. Например, в воде (Н2O - полярная молекула) хорошо растворяются низшие спирты, альдегиды, карбоновые кислоты. их высокую растворимость объясняют тем, что функциональные группы молекул этих веществ - гідроксильна-ВОН, альдегидная-СНВ, карбоксильная-СООН - являются полярными (однако с увеличением количества атомов Углерода в соответствующих молекулах их растворимость уменьшается). И наоборот, углеводороды (неполярные) смешиваются друг с другом в любых соотношениях. В воде такие вещества плохо растворяются или не растворяются совсем. Йод И2 (молекула неполярна) в воде не растворяется совсем, но хорошо растворяется в органических растворителях.
Некоторые соединения имеют неограниченную растворимость (спирт в водеj сульфатная кислота в воде), а другие растворяются в ограниченных количествах. Важной характеристикой раствора является его концентрация.
Концентрацией раствора называют количество растворенного вещества в единице массы или объема раствора1.
Во время растворения кристалла в жидкости молекулы (или ионы) вещества отрываются от кристалла и диффундируют между молекулами растворителя. Как только началось растворение, наблюдается и обратный процесс - кристаллизация. По мере роста концентрации растворенного вещества процесс растворения замедляется, а процесс кристаллизации ускоряется. Когда скорости обоих процессов выравниваются, и устанавливается их динамическое равновесие, раствор становится насыщенным. Насыщенный раствор - это раствор, в котором при определенной температуре данное вещество больше не может растворяться.
Часто концентрацию насыщенного раствора (при определенной температуре) выражают через массу вещества в 100 г растворителя (обычно воды) и называют коэффициентом растворимости, ks («ка-эс»). Так, запись 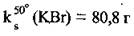 означает, что в 100 г воды при температуре 50 °С может раствориться не более 80,8 г калия бромида.
означает, что в 100 г воды при температуре 50 °С может раствориться не более 80,8 г калия бромида.
Данные о растворимости самых известных веществ в воде (в 100 г воды при температуре 20 °С) сведены в «Таблицу растворимости кислот, оснований и солей в воде» (см. Приложение 3). Хорошо растворимыми веществами (в таблице обозначено буквой «Г») считают такие, коэффициент растворимости которых более чем 10 г, малорастворимыми («М») - растворимость которых от 10 до 0,01 г, нерастворимыми («Н») - менее чем 0,01 г.
При определенных условиях (например, постепенно и осторожно охлаждая насыщенный раствор) можно получить перенасыщенный раствор2, когда концентрация растворенного вещества в перенасыщенных растворах больше, чем у насыщенных. Длительное время (в покое) такой раствор может существовать без изменений. Но если его встряхнуть или внести в него кристаллик растворенного вещества, т. н. зерно кристаллизации, начинается активный процесс кристаллизации избытка растворенного вещества3.
В соответствии ненасыщенный раствор - это раствор, в котором при определенной температуре данное вещество еще может растворяться (обычно с ним и имеют дело). Понятно, что концентрация растворенного вещества в ненасыщенных растворах меньше, чем у насыщенных.
Выражать концентрацию можно по-разному. Удобной характеристикой раствора является массовая доля w, поскольку с ее помощью можно легко определять массу растворенного вещества m в растворе и массу раствора m(р-ну):
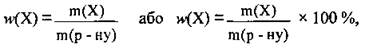
где w(X) - массовая доля растворенного вещества X,
m(Х) - масса растворенного вещества X, г,
m(р-ну) - масса раствора, г.
Молярная концентрация показывает, какое количество растворенного вещества содержится в 1 л раствора:
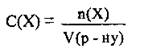
где С(Х) - молярная концентрация (молярність раствора вещества Х, моль/л,
n(Х) или v(X) -^- количество вещества X в растворе, моль,
V(р-ну) - объем раствора, л.
Так 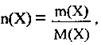 то
то
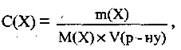
где С(Х) - молярная концентрация (молярність раствора вещества X, моль/л,
m(Х) - масса растворенного вещества X, г,
М(Х) - молярная масса вещества X, г/моль,
V(р-ну) - объем раствора, л.
Раствор, в 1 литре которого содержится 1 моль растворенного вещества, называют молярным (равно молярным)4. Обозначается буквой «М». Например, запись 1 М (КОН) - одномолярний раствор едкого кали - означает, что 1 л раствора содержит 1 моль вещества КОН, т.е. 56 г.
Важной для расчетов величиной является плотность раствора. Между плотностью растворов и их составом зависимость, которую отражают в графиках, таблицах. Состав раствора определенного вещества можно определить, если измерить его плотность. Абсолютную плотность раствора ρ («ро») определяют отношением его массы m к объему V:
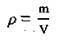
Относительную плотность жидких растворов измеряют с помощью ареометрів. Она означает отношение плотности раствора к плотности дистиллированной воды. Плотность растворов зависит от температуры (температура измерения указана на каждом ареометрі, градуировки простых ареометрів проводят при температуре 20 °С).
_____________________________________________________
1 Исторически пользуются разными понятиями концентрации раствора, например массовой концентрацией, то есть единицами массы растворенного вещества содержится в 100 единицах массы раствора. В быту часто используют понятие объемной концентрации или объемного процента (% об.), то есть соотношение объемов растворенного вещества (жидкой) и раствора. Согласно правилам IUPAC отношение массы или количества растворенного вещества к единице объема раствора называют концентрацией растворенного вещества.
2 Открыл 1784 г. начал изучать это явление, ввел термин перенасыщенный раствор российский академик (немецкого происхождения) Иоганн Тобиас Ловіц (1757-1804).
3 В бытовых химических грілках используют натрий ацетат. Во время нагрева до 100 °С (обычно в сосуде с кипящей водой) натрий ацетат тригидрат (температура плавления - 58 °С) плавится и переходит в водный раствор натрий ацетата. Во время охлаждения образуется его перенасыщенный раствор, который хранится при комнатной температуры без образования твердой фазы. Нажатие на специально вмонтированный металлический диск вызывает образования центра кристаллизации внутри грелки: перенасыщенный раствор переходит в твердую фазу. Процесс кристаллизации сопровождается выделением значительного количества теплоты - около 264-289 кДж/кг.
4 в Соответствии раствор, вич которого содержится 0,1 моль вещества, называют децимолярним, 0,01 моль - сантимолярним, 0,001 - мілімолярним.