КИСЛОТЫ
И ОСНОВЫ
2. Протолітична
равновесие
2.4. Водородный показатель растворов солей
Много
солевых растворов имеют нейтральную среду, некоторые - кислая или щелочная. По
Бренстедом, вода при этом выполняет функцию основания или кислоты.
Пример.
Натрий хлорид
Ион
Na+: не вступает в реакцию с водой.
Ион
Сl-: чрезвычайно слабое основание, поэтому
протоліз не происходит.
Раствор
натрий хлорида имеет нейтральную среду.
Пример.
Аммоний хлорид Ион NH4+: реагирует
с водой как слабая кислота
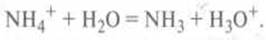
Ион
СИ-: очень слабая основа, поэтому протоліз не происходит.
Раствор
аммоний хлорида имеет кислую среду.
Пример.
Натрий карбонат
Ион
Na+: не вступает в реакцию с водой./o:p>
Ион
СО32-: реагирует с водой как слабая основа:
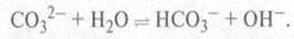
Раствор
натрий карбоната имеет щелочную среду.
Реакцию
солей с водой называют гидролизом. К тому же в зависимости от химической природы ионов
соли образуются кислые или щелочные растворы.