Ненасыщенные углеводороды (алкены, алкіни)
Ненасыщенными называются углеводороды, имеющие хотя бы один
двойной или
тройной (кратный) карбон-карбонний зв'язок.
Алкены
Углеводороды, принадлежащие к гомологического ряда
алкенов (непредельных углеводородов ряда этилена), имеют один двойной карбон-карбонний связь. В их названии суффикс
-ан заменяется на
-ен.
Например: етен (этилен):
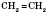
пропен (пропилен):
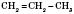
Первый представитель гомологического ряда алкенов -
етилен.
Электронная формула:
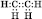
Структурная формула:
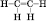
Общая формула алкенов - C
nH2
n.
Алкіни
Еще один гомологический ряд ненасыщенных углеводородов -
алкіны, имеющие тройные связи. Названия алкінів происходят от названий алканов, при этом суффикс -
ан замещается на суффикс
-ин.
Первый представитель гомологического ряда алкінів -
ацетилен 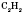
.
Электронная формула:
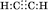
Структурная формула:
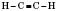
Общая формула алкінів -
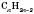
.
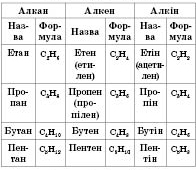
Представители гомологических рядов алканов, алкенов, алкінів
Изомерия алкенов и алкінів
В ненасыщенных углеводородов кроме
изомерии по углеродным скелетом появляется новый вид изомерии -
изомерия по положению кратной связив. Положения кратной связи указывается цифрой в конце названия углеводорода.
Например:
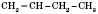
- бутен-1;
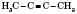
- бутин-2.
Считают атомы Карбона с той стороны, к которой ближе кратный связь. Например:
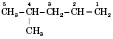
4-метилпентен-1
Этилен и ацетилен
Физические свойства этилена и ацетилена. Газы без цвета и запаха, мало растворимые в воде, немного легче воздуха.
Получение непредельных углеводородов.
1) Ненасыщенные углеводороды можно получить дегідруванням насыщенных. Реакция идет в присутствии катализаторов (платины или никеля) и при нагревании. В зависимости от степени дегидрирования можно получить алкены или алкіни, а также осуществить переход от алкенов к алкінів:
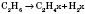
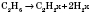
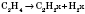
2) При крекинге алканов получается смесь алканов и алкенов, например:
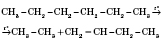
3) Ацетилен в промышленности и лаборатории получают взаимодействием кальций карбида с водой, реакция экзотермическая:
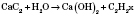
4) В промышленности ацетилен в основном получают термическим разложением метана:
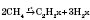
5) Дегідрогалогенування галогеналканів нагреванием со спиртовым раствором щелочи - лабораторный метод получения непредельных углеводородов:
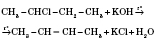
Реакция идет по
правилу Зайцева:
Водород в реакциях разложения отщепляется от того атома Углерода, у которого наименьшее количество атомов Водорода:
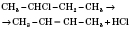
(Водород отщепляется от
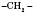
, но не от
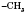
)
Химические свойства этилена и ацетилена. Для этилена и его гомологов характерны реакции, идущие с разрывом одной из двойных соединений и присоединением атомов по месту разрыва, то есть реакции присоединения.
1) Горение (в достаточном количестве кислорода или воздуха):
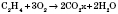
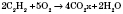
2) Гидрирование (присоединение водорода):
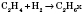
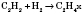
;
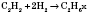
3) Галогенування (присоединение галогенов):
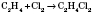
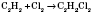
;
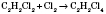
4) Гідрогалогенування (присоединение галогеноводородов):
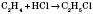
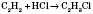
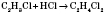 Качественной реакцией на непредельные углеводороды
Качественной реакцией на непредельные углеводороды является обесцвечивание бромной воды или раствора калий перманганата. При взаимодействии бромной воды с ненасыщенными углеводородами происходит присоединение брома по месту разрыва кратных связей и, соответственно, исчезновения окраски, которое было обусловлено растворенным бромом:
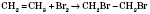 Правило Марковников
Правило Марковникова: Водород присоединяется к тому атому Углерода, который связан с большим числом атомов Водорода. Это правило можно показать на реакциях гидратации несимметричных алкенов и гідрогалогенування:
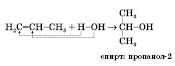
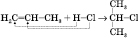
2-хлорпропан
При взаимодействии галогеноводородов с алкінами присоединения второй молекулы галогеноводню идет согласно
правила Марковникова:
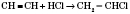
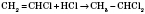
Применение этилена и ацетилена. Ненасыщенные углеводороды используют для синтеза многих органических веществ.
Этилен используют для получения этилового спирта, полиэтилена. Он ускоряет созревание плодов.
Ацетилен используют для автогенной сварки металлов.
Полимеры
Для ненасыщенных соединений характерны реакции полимеризации.
Полимеризация - это последовательное соединение молекул низкомолекулярной вещества с образованием высокомолекулярного вещества. При этом соединение молекул происходит по месту разрыва двойных связей.
Например, полимеризация этилена:
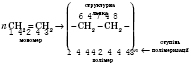
Продукт полимеризации называется
полимером, а исходное вещество, вступающее в реакцию, -
мономером; повторяющиеся в полимере группировки называются
структурными или
элементарным звеньямы; число элементарных звеньев в макромолекулі называется
степенью полімеризацій.
Название полимера складывается из названия мономера и приставки
поли-, например полиэтилен, поливинилхлорид, полистирол.
В зависимости от степени полимеризации тех же мономеров можно получать вещества с различными свойствами. Например, полиэтилен с короткими цепями
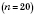
является жидкостью, что имеет смазочные свойства. Полиэтилен с длиной цепи в 1500-2000 звеньев - твердый, но гибкий пластический материал, идущий на изготовление пленки, посуды, бутылок. Полиэтилен с длиной цепи в 5-6 тыс. звеньев является твердым веществом, из которого можно готовить литые изделия, трубы.
В расплавленном состоянии полиэтилена можно придать любую форму, которая сохраняется после отверждения. Такое свойство называется
термопластичністю.