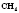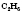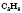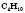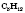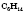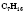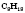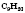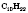Насыщенные углеводороды (алканы)
Метан
Простейшая органическое вещество -
метан - имеет молекулярную формулу
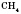
.
Структурная формула метана:
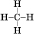
Электронная формула метана:
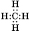
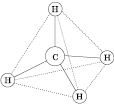
Молекула метана имеет форму тетраэдра: в центре - атом Углерода, в вершинах - атомы Водорода,
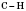
соединения направлены к вершинам тетраэдра под углом
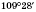
.
Физические свойства метана. Газ без цвета и запаха, легче воздуха, малорастворим в воде.
Распространение метана в природе. В природе метан образуется при гниении растительных остатков без доступа воздуха.
Метан является основной составной частью природного газа.
Получение метана.
1) С натрий ацетата:
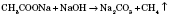
2) Синтезом из углерода и водорода (400-500
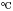
и повышенное давление):
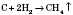
3) С алюминий карбида:
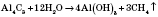
Химические свойства метана.
1) Горение:
- при достаточном количестве кислорода образуется углекислый газ и вода:
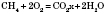
- при недостаточном количестве кислорода образуется угарный газ и вода:
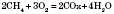
- или углерод и вода:
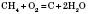
Смесь метана с воздухом взрывоопасна.
2) Термическое разложение без доступа кислорода на углерод и водород:
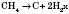
.
3) Взаимодействие метана с галогенами, в частности хлором, проходит по цепным
вільнорадикальним механізмом.
В молекулах хлора под действием света происходит разрыв связей и образуются свободные радикалы хлора:
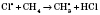
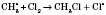
По типу эта реакция относится к реакциям замещения.
В результате хлорирования могут образовываться хлорметан
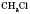
, дихлорметан
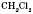
, трихлорметан (хлороформ)
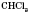
, тетрахлорметан (четыреххлористый карбон)
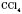
.
Применение метана. Метан в больших количествах расходуется в качестве топлива. Из него получают водород, ацетилен, сажу. Он используется в органических синтезах, в частности, для получения формальдегида, метанола, муравьиной кислоты и других синтетических продуктов.
Гомологический ряд алканов
Гомологический ряд метана имеет несколько названий:
алканы,
или
насыщенные вуглеводни
, парафини. Состав молекул всех членов гомологического ряда может быть выражен одной общей формуле. Для алканов это формула
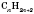
.
Представители гомологического ряда алканов
| Название | Молекулярная формула |
| Метан | 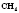 |
| Этан | 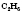 |
| Пропан | 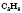 |
| Бутан | 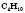 |
| Пентан | 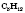 |
| Гексан | 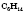 |
| Гептан | 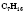 |
| Октан | 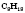 |
| Нонан | 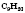 |
| Декан | 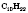 |
Изомерия.
Изомерия - это явление, при котором вещества одинакового состава имеют различную пространственную структуру и, соответственно, свойства.
Изомеры имеют одинаковый состав, но разное строение.
По заместительной номенклатуре основой для названия служит один
карбонний цепьюг, а все остальные фрагменты молекулы рассматриваются как
заместительи. Заместителями могут быть свободные радикалы, образованные алканами.
Радикалы, образованные алканами
| Алкан | Радикал |
| Формула | Название | Формула | Название |
| Метан | | Метил |
| Этан | | Этил |
| C3H8 | Пропан | | Пропил |
| Бутан | | Бутил |
Чтобы дать название ізомерови, нужно:
- выделить цепь с наибольшим количеством атомов Углерода -
главный цепьюг, посчитать в ней количество атомов Углерода; соответствующее название углеводорода будет основой названия изомерам;
- определить, к какому по счету атома Карбона прикрепляется
радикал. Это значение будет записано цифрой в начале названия;
- определить название радикала с числом атомов Углерода в нем.
Потом дописываются атомы Водорода.
Например:
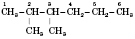
2, 3-диметилгексан
Физические свойства алканов. При обычных условиях первые четыре члена гомологического ряда алканов
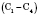
- газы. Нормальные алканы от пентана до гептадекану
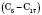
- жидкости, начиная с
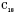
и выше - твердые вещества.
По мере увеличения числа атомов в цепи, т.е. с ростом относительной молекулярной массы, возрастают температуры кипения и плавления алканов.
Алканы практически нерастворимы в воде, потому что их молекулы малополярні и не взаимодействуют с молекулами воды, но хорошо растворяются в неполярных органических растворителях, таких как бензен, тетрахлорметан. Жидкие алканы легко смешиваются друг с другом.
Получение алканов.
1) Гидрирование (присоединение водорода) непредельных углеводородов:
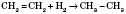
2)
Реакция Вурца, что служит для увеличения карбонного цепи:
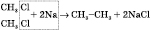
или
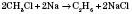
Химические свойства алканов.
1) Не вступают в реакции присоединения.
2) Горят:
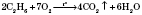
3) Разлагаются при нагревании:
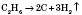
4) Вступают в реакции галогенування (реакции замещения):
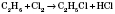
5) При нагревании и под действием катализаторов происходит
крекинг - гомолітичний разрыв С-С связей. При этом образуются алканы и низшие алканы, например:
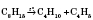
6) При дегідруванні метана и этилена образуется ацетилен
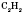
:
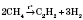
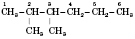
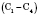 - газы. Нормальные алканы от пентана до гептадекану
- газы. Нормальные алканы от пентана до гептадекану 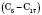 - жидкости, начиная с
- жидкости, начиная с 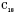 и выше - твердые вещества.
и выше - твердые вещества.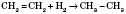
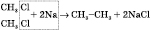
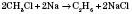
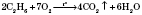
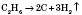
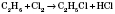
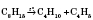
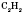 :
: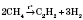
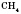 .
.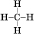
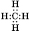
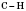 соединения направлены к вершинам тетраэдра под углом
соединения направлены к вершинам тетраэдра под углом 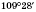 .
.
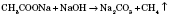
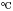 и повышенное давление):
и повышенное давление):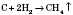
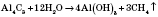
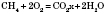
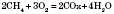
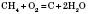
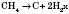 .
.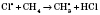
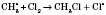
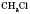 , дихлорметан
, дихлорметан 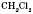 , трихлорметан (хлороформ)
, трихлорметан (хлороформ) 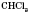 , тетрахлорметан (четыреххлористый карбон)
, тетрахлорметан (четыреххлористый карбон) 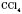 .
.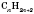 .
.