ЧАСТЬ И
ОБЩАЯ ХИМИЯ
ХИМИЧЕСКИЕ РЕАКЦИИ И ЗАКОНОМЕРНОСТИ ИХ
ТЕЧЕНИЯ
Классификация по тепловым эффектом
По
тепловым эффектом реакции относятся или к экзотермических (реакции с выделением
теплоты) или эндотермических (реакции с поглощением теплоты).
Тепловой эффект химической реакции. Термохимические уравнения
Большая
количество химических процессов происходит с выделением энергии, в частности горения
(реакция, которая происходит с выделением теплоты и света). Существует и немало других
реакций, при прохождении которых выделяется теплота.
Есть
реакции, в которых теплота поглинається. их осуществление требует нагрева. К
таких реакций относятся реакции разложения гидроксидов, оксигеносодержащих кислот,
их солей, кристаллогидратов:
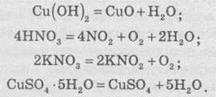
Если
прекратить нагревание, то прекращается и реакция. С другой стороны, реакции, которые
протекают с выделением теплоты, часто происходят самопроизвольно. Правда, в
большинстве случаев их надо инициировать (например, поджечь вещество), после чего
они будут проходить без посторонней помощи.
Все
реакции происходят с определенным тепловым эффектом - или с выделением теплоты, или
с его поглощением. Если количество теплоты незначительная, то заметить тепловой эффект
реакции довольно трудно.
Реакции,
в которых теплота выделяется, называются экзотермическими, а реакции, в которых теплота
поглощается,- ендотермічними.
Показать
выделение или поглощение теплоты можно в химическом уравнении:
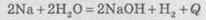
(«+Q» означает, что
теплота выделяется);
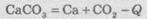
(«-Q» означает, что теплота поглощается).
Причина выделения или поглощения
теплоты при химической реакции
Каждая
вещество имеет свою внутреннюю энергию, которую невозможно измерить. Она состоит из
энергий всех частиц вещества - атомов, молекул, ионов и энергий химических
связей между ними. Энергия каждой частицы в свою очередь имеет несколько составляющих.
Среди них - кинетическая энергия, потому что частица может двигаться, вращаться (если
вещество является газом или жидкостью) или колебаться (если вещество твердое), и энергия
электронов в атоме. Если суммарная внутренняя энергия реагентов превышает суммарную
внутреннюю энергию продуктов, то разница энергии выделяется во время реакции в
виде тепла, а если она ниже, то происходит поглощение теплоты. Разница
этих энергий и составляет тепловой эффект реакции.
Тепловой
эффект реакции зависит от нескольких факторов. Один из них - это природа веществ,
участвующих в реакции. Так, расписание нитроген(II) оксида происходит с
выделением теплоты:
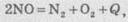
а меркурий(ІІ) оксида - с поглощением
теплоты:
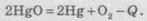
Второй
фактор - это масса веществ. Чем больше масса веществ, тем больше выделяется или
поглощается теплоты.
Если
букву «Q» заменить числовым значением теплового
эффекта, то мы получим термохімічне уравнения:
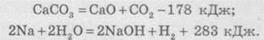
Записанное
в первом уравнении значение теплового эффекта соответствует участия в реакции 1 моль
кальций карбоната и образованию 1 моль кальций оксида и 1 моль карбон(ИV) оксида.
Большая
количество реакций, в случае изменения условий, могут происходить в противоположных
направлениях. Так, кальций карбонат при нагревании разлагается, а при обычных
условиях происходит обратная реакция - кальций оксид реагирует с углекислым газом:
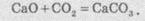
Эта
реакция в отличие от эндотермической реакции разложения кальций карбоната
проходит с выделением теплоты, т.е. является экзотермической. Значение ее теплового
эффект будет таким же, но с противоположным знаком:
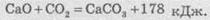
Тепловой
эффект прямой реакции равен тепловому эффекту обратной реакции, но имеет противоположный
знак.