ЧАСТЬ И
ОБЩАЯ ХИМИЯ
ХИМИЧЕСКИЕ РЕАКЦИИ И ЗАКОНОМЕРНОСТИ ИХ
ТЕЧЕНИЯ
Классификация
химических реакций
Классификация по числу и составу
исходных реагентов и продуктов реакции
Реакция
сообщения - реакция, в результате которой из нескольких веществ с относительно простым
составом образуется одна большая вещество с более сложной структурой.
А
+ В + С = D.
Как
правило, такие реакции сопровождаются выделением тепла. Наиболее характерные
реакции соединения для взаимодействия простых веществ:
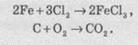
Также
они характерны и для сложных соединений. Например, для реакций взаимодействия оксидов
с водой или основным оксидом с кислотным.
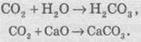
Реакции разложения приводят к образованию нескольких веществ с
одного сложного вещества:
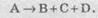
Продуктами реакции разложения могут быть
как сложные вещества, так и простые:
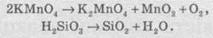
В реакциях замещения атом одного
элемента замещает атом или группу атомов в сложном соединении:

В реакциях замещения обычно одна
простое вещество реагирует со сложной с образованием другого простого вещества и другой
соединения:
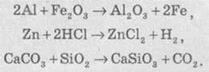
К реакциям обмена относятся реакции, в
которых два вещества обмениваются своими составными частями (атомами или группами
атомов):
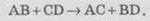
Это самая распространенная группа реакций между
состав ими веществами, в частности, между кислотами, основаниями и оксидами.
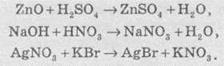
Обычно эти реакции происходят тогда,
когда в результате образуется газувата вещество, осадок или малодисоціювальна
вещество, в частности вода.
Классификация по числу фаз, в которых находятся участники реакций
Реагенты, участвующие в химической
реакции, могут находиться в одинаковых агрегатных состояниях и разных. В зависимости от
того, существует граница раздела между реагентами, реакции разделяют на две группы.
Гомогенные реакции. К ним относятся
реакции между газуватими веществами или между растворенными веществами.
Гетерогенные реакции. К ним относятся
реакции, в которых реагенты находятся в разных фазах (т.е. между веществами существует
граница раздела). Например:
Реакции между газом и жидкостью:
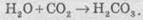
Реакции между газами и твердыми
веществами:

Реакции между твердыми веществами и
жидкостями (растворами):

Классификации
по возможности протекания реакции в прямом и обратном направлениях
Оборотными
называют реакции, продукты которых способны реагировать друг с другом в тех же
условиях, в которых они получены, с образованием исходных веществ. Например, при
нагревании йодоводню до температуры 500 °С 24% его распадается на йод и
водород: 2НІ →
Н2 + И2.
Если
же в том же пространстве нагреть одинаковые количества йода и водорода до 500 °С, то
76 % их соединяются и образуют йодоводень:

Для
обратимых реакций в уравнении принято записывать вместо знака равенства
двунаправленную стрелку. Этим подчеркивают, что в тех же условиях проходит как
прямая реакция, так и оборотная.
Необратимыми
называют такие химические процессы, продукты которых не способны реагировать друг с другом
с образованием исходных веществ. Примерами необратимых реакций могут служить реакции
расписания калий перманганата при нагревании:

Органические
реакции в большинстве случаев являются обратимыми, в отличие от неорганических.