Основные типы химической связи:
ковалентная (полярная, неполярная), ионный, металлический, водородный.
Ковалентная связь
Ковалентная связь - это химическая связь, которая осуществляется между атомами за счет электронных пар, в одинаковой мере принадлежащих обоим атомам. Ковалентная связь образована одинаковыми атомами (с одинаковой електронегативністю), называется
неполярним, а образованный различными атомами (с разной електронегативністю), -
полярним.
Электроны, способные участвовать в образовании химической связи, называются
валентными. Их количество определяет число связей, образуемых атомом, то есть
валентність.
У элементов главных подгрупп валентными являются электроны последнего энергетического уровня, у элементов побочных подгрупп - последнего и предпоследнего уровней.
При образовании химической связи атомы отдают, получают или усуспільнюють с другими атомами электроны так, чтобы образовалась устойчивая электронная конфигурация атомов инертных газов (октет электронов).
Образования ковалентной неполярной связи на примере молекулы водорода).
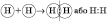
Электронная плотность в данном случае не смещена ни к какому из атомов, поскольку они имеют одинаковую электроотрицательности. На одном из атомов не сосредоточен положительный или отрицательный заряд, то есть молекула не имеет полюсов.
Образования ковалентной полярной связи (на примере молекулы водород фторида).
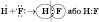
Электронная плотность смещена к атому Фтора как более электроотрицательного элемента. Поэтому атом Фтора будет частично отрицательный заряд, а Водород - частично положительный:
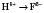
.
Молекула HF имеет положительный (атом Водорода) и отрицательный (атом Фтора) полюса, то есть она полярная.
Донорно-акцепторный механизм образования химической связи состоит в том, что связь образуется в результате перехода уже существующей электронной пары
атома-донора в общее пользование донора и
атом-акцептора, который предоставляет свободную электронную орбиталь.