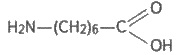Часть III. ОРГАНИЧЕСКАЯ ХИМИЯ
Раздел 18.
АЗОТСОДЕРЖАЩИЕ ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
§
18.4. Аминокислоты
Аминокислотами называются органические
соединения, в молекулах которых содержатся одновременно аминогруппа - NH2 и карбоксильная группа - СООН.
их можно рассматривать как производные
карбоновых кислот, которые образуются замещением одного или нескольких атомов водорода в
углеводородном радикале на аминогруппы. Например:
СН3СООН;
H2N-СН2-СООН.
Уксусная
кислота
Амінооцтова кислота
Названия
аминокислот образуются от названий соответствующих кислот с добавлением префикса
амино-. Однако аминокислоты, которые входят в состав белков, имеют также практические
названия, сложившиеся Исторически, например амінооцтова кислота еще называется
гликоколом, или глицином, амінопропіонова - аланином и т. д.
Изомерия аминокислот зависит от
размещение аминогруппы и строения углеводородного радикала. За размещением
аминогруппы (относительно карбоксильной) различают: а-аминокислоты (аминогруппы
расположены возле первого атома углерода, считая от карбоксильной группы),
(β-аминокислоты (аминогруппа находится у второго атома углерода),
в-аминокислоты (аминогруппа находится у третьего атома углерода) и т. д.
Например:
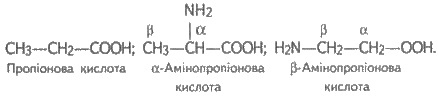
Изомерия обусловлена разветвлением
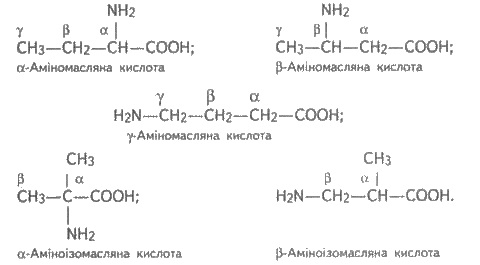
углеводородного радикала, была рассмотрена ранее. Для примера напишем формулы
соединений состава С3Н6(NН2)СООН:
Важнейшее значение имеют
а-амінокарбонові кислоты. Они широко распространены в природе - из них
построены белки. С гидролизом белков выделено 22 а-аминокислоты.
Аминокислоты - бесцветные кристаллические
вещества, плавящиеся с разложением при высоких температурах (свыше 250°С).
Легкорастворимые в воде и нерастворимые в эфире. По химическим свойствам
аминокислоты - своеобразные органические амфотерные соединения. Амфотерные свойства
объясняются взаимным влиянием аминогруппы и карбоксильной группы в молекулах
аминокислот:
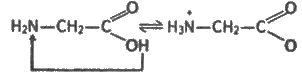
Это можно объяснить так. Карбоксильная
группа аминокислоты отщепляет ион водорода, который затем присоединяется к аминогруппе
той самой молекулы по месту неподеленной электронной пары азота. В результате
действие функциональных групп нейтрализуется, образуется так называемая внутренняя соль,
в растворе нет избытка ионов водорода или гидроксила, а поэтому он не действует на
индикатор. В водных растворах а-аминокислоты существуют в виде внутренней соли,
или биполярного иона:
+
H3N-СН2-СOO- .
А поскольку раствор содержит ионы, он проводит
электрический ток.
Однако растворы тех аминокислот, в
молекулах которых содержится неодинаковое количество аминогрупп и карбоксильных групп,
действуют на индикаторы. Так, например, водный раствор глутаминовой кислоты
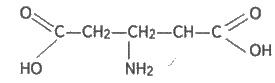
имеет
слабокислую реакцию (преобладает количество карбоксильных групп), а водный раствор
лизина
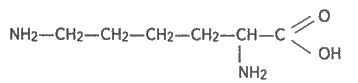
слабощелочную
(преобладают аминогруппы). Амфотернии характер аминокислот подтверждается
взаимодействием их со щелочами и кислотами с образованием солей. Например:
H2N-CH2-COOH + NaOH -> H2N-СН2-COONa + Н2О
Натриевая соль глицина
и
H2N-СН2-СООН + НСl -> НСl ∙ H2N-СН2-СООН.
Хлористоводородная
соль глицина
Следовательно, при повышении концентрации
ионов ОН- аминокислоты реагируют в форме аниона (как кислота), а при
повышении концентрации ионов Н+ - в форме катиона (как основа),
т.е.
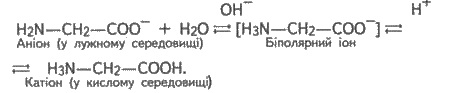
Аминокислоты взаимодействуют с металлами,
оксидами металлов, образуя соли, а также со спиртами, образуя сложные эфиры.
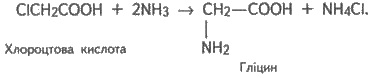
Аминокислоты образуются во время
гидролиза белков как конечные продукты гидролиза. Однако их можно добыть и
синтетически, например при взаимодействии аммиака с галогеннозамещенными кислотами.
Последние добывают хлорированием:
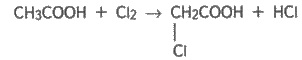
и
далее:
Аминокислоты необходимы для построения белков
живого организма. Люди и животные получают их в составе белковой пищи. Много
аминокислот применяются в медицине как лечебные средства, а некоторые - в
сельском хозяйстве для подкормки животных. Неразветвленные аминокислоты, как
бифункциональные (содержат две функциональные группы) мономеры, используемые
для производства синтетических волокон, в том числе капрона и енанту.
Рассмотрим извлечения полимера, с
которого производят капроновое волокно. Первым этапом является поликонденсация
ε-аминокапроновой кислоты
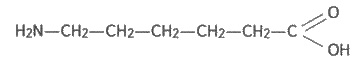
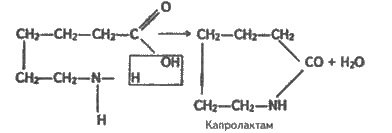
В производстве капронового волокна
применяют не непосредственно ε-аминокапроновую кислоту, а ее производное -
капролактам, который является продуктом взаимодействия функциональных групп молекул кислоты:
Во время синтеза под воздействием воды
молекулы капролактама превращаются в молекулы ε-аминокапроновой
кислоты, которые подвергаются поликонденсации:
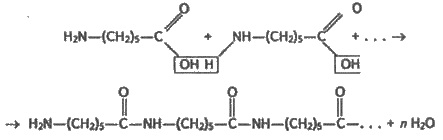
Как видно из формулы, молекула
полимера, образуется, состоит из остатков ε-аминокапроновой
кислоты, которые многократно повторяются, а связи между остатками возникают
вследствие отщепления молекул воды.
Строение добытого полимера можно
изобразить формулой
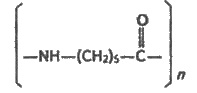
Он имеет вид смолы. Для
производства волокон смолу плавят, пропускают через фильеры, далее подвергают волокна
специальной обработке, после чего скручивают в нити. Изделия из капрона широко
применяются в быту. Капроновую смолу используют для изготовления прочных
и устойчивых к износу деталей машин и механизмов.
Енант
добывают поликонденсацией ω-аміноенантової кислоты: