ОРГАНИЧЕСКИЕ РЕАКЦИИ
3. Ионные реакции
3.4. Електрофільне замещение
Характерной
реакцией бензену и других ароматических соединений является електрофільне замещения, при
котором ароматическая система сохраняется:
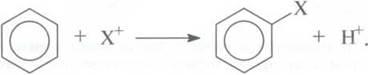
Електрофільне
замещение в ароматических соединениях проходит в три этапа.
1-й этап: получение активной електрофільної
частицы (Х+) преимущественно с помощью катализатора.
2-й этап: електрофільна частица «атакует»
отрицательно заряженный π-электронную
облако бензену, образуя π-комплекс.
С я-комплекса медленно формируется переходное состояние положительно заряженного σ-комплекса.
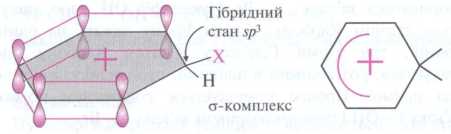
3-й
этап: образуется продукт с відщеплюванням протона.
Пример.
Галогенування бензену
Молекулы
галогена не електрофільні. Следовательно, с них нужно получить електрофільні
частички. Это происходит при их соединении с кислотами Льюиса, как, например, с
ферум(ІІІ) бромидом:

Процесс электрофильного замещения
начинается с взаимодействия электрофильного иона Брома с я-электронной облаком
ароматической системы.

Електрофіл
йон Вr+
вытягивает с я-электронной ароматической системы электронную пару, образуя за ее
помощью ковалентная σ-связь
с одним из атомов Углерода, что приводит к образованию σ-комплекса.

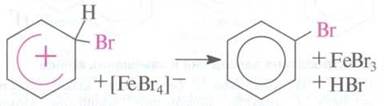
Вследствие
отщеплению протона ароматическая система восстанавливается. Протон реагирует с ионом [FeBr4]-, образуя феррум(III) бромид и водород
бромид.
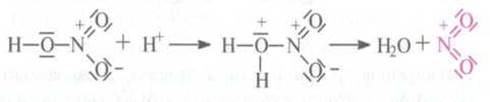
Нитрования
ароматических соединений происходит аналогичным образом. Для этого нужна нітруюча
смесь с концентрированной азотной кислоты и концентрированной серной кислоты.
Добавление серной кислоты протонує нитратную кислоту. В результате
образуется сильный електрофільний нітроній-ион, NO2+.