Часть II.
НЕОРГАНИЧЕСКАЯ ХИМИЯ
Раздел 13. МЕТАЛЛЫ
ГЛАВНЫХ ПОДГРУПП
§
13.9. Жесткость воды и способы ее устранения
В природе чистой воды не бывает: она
всегда содержит примеси каких-либо веществ. В частности, взаимодействуя с солями,
содержащиеся в земной коре, она приобретает определенной твердости.
Жесткость воды - совокупность
свойств, обусловленных содержанием в воде катионов кальция Са2+ и
катионов магния Мg2+. Если концентрация этих катионов
велика, то воду называют жесткой, если мала - мягкой. Именно они придают
специфических свойств природным водам. При стирке белья в жесткой воде
ухудшается качество тканей и повышения щуються расходы милая, необходимого на
связывание катионов Са2+ и Мg2+:
2С17Н35СОO- + Са2+ = (С17Н35СОО)2
Са↓;
2С17Н35СОО-
+ Мg2+ = (С17Н35СОО)2
Мg↓,
и
пена образуется лишь после полного осаждения этих катионов. Правда, некоторые
синтетические моющие средства хорошо моют и в жесткой воде, поскольку их кальциевые и
магниевые соли легко растворяются. В жесткой воде плохо развариваются пищевые
продукты, сваренные в ней овощи невкусные. Очень плохо заваривается чай, и вкус
его теряется. В то же время в санитарно-гигиеническом отношении эти катионы не является
опасными, хотя при высоком содержании катионов Мg2+ (как в море или океане) вода
горьковатая на вкус и оказывает послабляющее действие.
Жесткая вода непригодна для
использования в паровых котлах: растворенные в ней соли во время кипячения
образуют на стенках котлов слой накипи, который плохо проводит теплоту. Это
приводит к перерасходу топлива, преждевременному износу котлов, а иногда, вследствие
перегрев котлов, и к аварии. Твердость воды вредна для металлических
конструкций, трубопроводов, кожухов охлаждаемых машин.
Катионы кальция Са2+
предопределяют кальциевую жесткость, а катионы Мg2+ - магниевую жесткость воды. Общая
твердость состоит из кальциевой и магниевой, то есть с суммарной концентрации
в воде катионов Са2+ и Мg2+.
Относительно процессов умягчения воды
различают жесткость карбонатную и некарбонатную. Карбонатной называется твеpдість, обусловленная наличием той
части катионов Са2+ и Mg2+, которая эквивалентна гідрокарбонатним
ионам НСО-3, содержащиеся в воде. Другими словами,
карбонатная жесткость вызвана наличием гидрокарбонатов кальция и магния. Под
при кипячении гидрокарбонаты разрушаются, а малорастворимые карбонаты,
образуются, выпадают в осадок, и общая жесткость воды уменьшается на
значение карбонатной жесткости. Поэтому карбонатную жесткость называют также
временной жесткостью. Во время кипячения катионы Са2+ оседают в
виде карбоната кальция:
Са2+ + 2НСO-3 = СаСО3 ↓
+ Н2О + СO2,
а
катионы магния Mg - в
виде основного карбоната или в виде гидроксида магния (при pH
> 10,3):
2Мg2+ + 2НСО-3 + 2OН- = (МgОН)2 СО3 ↓
+ Н2О + СО2
(гидроксид-ионы
ВОН образуются за счет взаимодействия ионов НСО- с водой: НСО-3
+ Н2O ⇆ Н2СО3 + ОН ).
И часть твердости,
сохраняющаяся после кипячения воды, называется некарбонатною. Она
определяется содержанием в воде кальциевых и магниевых солей сильных кислот,
преимущественно сульфатов и хлоридов. При кипячении эти соли не удаляются, а
поэтому некарбонатную жесткость называют также постоянной твердостью.
Рассмотрим количественную характеристику
жесткости воды. Степень жесткости воды выражается по-разному. В нашей стране
ее выражают числом міліеквівалентів (мэкв) катионов Са2+ и Мg2+, содержащихся в 1 л воды. Поскольку
1 мэкв жесткости соответствует содержанию 20,04 мг/л катионов С2+а или
12,16 мг/л катионов Мg2+, то, согласно определению, общую
твердость воды Т (мэкв/л) можно вычислить по формуле:
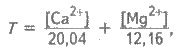
где
[Са2+ ] и [Mg2+ ] - концентрации ионов Са2+
и Mg2+ , мг/л.
По значению жесткости природную воду
различают как очень мягкую - с твердостью до 1,5; мягкую - от 1,5 до 4; средней
твердости - от 4 до 8; жесткую - от 8 до 12 и очень жесткую - свыше 12 мэкв/л.
Жесткость воды хозяйственно-питьевых
водопроводов не должна превышать 7 мэкв/л (ГОСТ 2874-82).
Очень часто жесткую воду перед
использованием смягчают. Обычно этого достигают обработкой воды различными
химическими веществами. Так, карбонатную жесткость можно устранить добавлением
гашеной извести:
Са2+ + 2НСО-3
+ Са2+ + 2OН-
= 2СаСО3↓+ 2Н2О;
Мg2+ + 2НСО-3 +
2Са2+ + 4OН-
= Мg(ОН)2↓
+ 2СаСО3 и + 2Н2O.
При
одновременном добавлении извести и соды можно избавиться от карбонатной и некарбонатної
твердости (известково-содовый способ). Карбонатная жесткость при этом устраняется
известью (см. выше), а некарбонатная - содой:
Са2+ + С02-3
= СаСО3↓; Мg2+ + СO2-3 = МgСО3
и дальше
МgСО3 + Са2+ + 2OН- = Мg(ОН)2 ↓
+ СаСО3 ↓.
Применяют и другие способы устранения
жесткости воды, среди которых один из самых современных основывается на применении катионитов
(катіонітний способ). Есть такие твердые вещества, которые содержат в своем составе
подвижные ионы, способные обмениваться на ионы внешней среды. Они достали
название ионитов. Особенно распространены ионообменные смолы, которые добывают на основе
синтетических полимеров.
Иониты (ионообменные смолы) разделяют
на две группы. Одни из них обменивают свои катионы на катионы среды и
называются катіонітами, другие обменивают свои анионы и называются аніонітами.
Иониты не растворяются в растворах солей, кислот и щелочей.
Катиониты имеют вид черных или
темно-бурых зерен диаметром от 0,5 до 2 мм (КУ-1, КУ-2, СБС и другие), анионита
- зернистые вещества белого, розового или коричневого цвета (АВ-16, АВ-17,
АН-2Ф и другие).
Для устранения жесткости воды
применяют катиониты - синтетические ионообменные смолы и алюмосиликаты,
например Na2 [l2Sи2В8 ∙ nН2O]. их состав условно можно выразить
общей формулой Na2R, где Na - достаточно подвижный катион и R2 - частичка катионита, что несет
отрицательный заряд. Так, в приведенном примере R2 = [Al2Si2O8 ∙ nН2O]2- .
Если пропускать воду сквозь слои
катионита, то ионы натрия будут обмениваться на ионы кальция и магния.
Схематически эти процессы можно выразить уравнениями:
Са2++ Na2R
=2Na+ + CaR;
Mg2++ Na2R = 2Na+ + MgR.
Следовательно, ионы кальция и магния переходят
из раствора в катионит, а ионы натрия - из катионита в раствор; при этом твердость
устраняется.
После
использование большей части ионов натрия катиониты обычно регенерируют -
выдерживают в растворе хлорида натрия, при участии которого происходит обратный
процесс: ионы натрия замещают в катіоніті ионы кальция и магния, которые переходят
в раствор:
CaR
+ 2Na+
= Na2R
+ Са2+; MgR
+ 2Na+
= Na2R + Mg2+.
Регенерированный катионит снова можно
использовать для смягчения новых порций жесткой воды.