РАЗДЕЛ II. НЕОРГАНИЧЕСКАЯ ХИМИЯ
9. Неметаллические элементы и их соединения. Неметаллы
9.3. Элементы VIA группы
9.3.8. Оксиды Серы
Сульфур(ИV) оксид
Сульфур образует два оксиды - сульфур(ИV) оксид и сульфур(V) оксид. Наибольшее значение среди соединений Серы со степенью окисления +4 имеет сульфур(ИV) оксид (сульфур диоксид, сернистый газ) SO2. Имеет молекулярные кристаллические решетки. В его молекуле Сульфур образует четыре ковалентные связи:
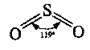
Физические свойства и физиологическое действие
Сульфур(ИV) оксид - бесцветный газ с резким удушливым запахом, ядовит. Тяжелее воздуха более чем в два раза. Хорошо растворяется в воде. В одном объеме воды растворяется 40 объемовS02.
Сульфур(ИV) оксид - очень токсичное вещество, это один из наиболее опасных загрязнителей окружающей среды. Он попадает в воздух при сжигании угля, окислении сульфидных руд. В воздухе он взаимодействует с водяными парами, образуя сульфітну кислоту, которая вместе с продуктом его окисления - сульфатной кислотой - вызывает появление кислотных дождей. Кислотные дожди отрицательно влияют на растительный мир, вызывают ряд заболеваний у живых существ, разрушают строительные сооружения.
Добыча сульфур(ИV) оксида
Лабораторные способы:
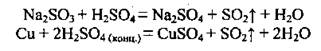
Промышленные способы:
• сжигание серы:
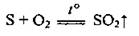
• обжиг пирита:
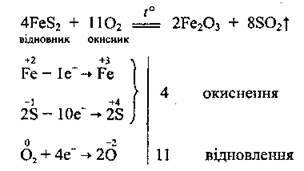
Химические свойства сульфур(ИV) оксида
Сернистый газ - это типичный кислотный оксид, которому соответствует сульфитная кислота.
1. Выявляет общие свойства кислотных оксидов. Он взаимодействует с водой, образуя сульфітну кислоту, с основными и амфотерными оксидами, с основаниями, образуя два типа солей: кислые (гідрогенсульфіти) и средние (сульфиты):
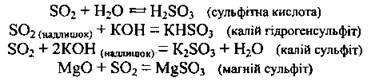
2. Сернистый газ проявляет свойства как окисника, так и восстановителя. Степень окисления Серы в SO2 является промежуточным (+4), а потому сульфур(ИV) оксид может быть и восстановителем, и окисником, а также может диспропорціонувати:
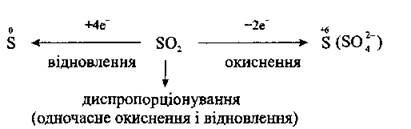
Реагируя с более сильными окислителями, SO2 проявляет восстановительные свойства:
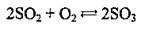
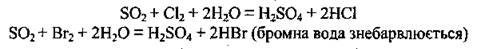
Реагируя с сильным восстановителем, SO2 становится окисником:
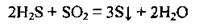
Сернистый газ диспропорціонує, если его пропустить через горячий концентрированный раствор щелочи:
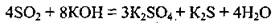
Восстановительные свойства в сульфур(ИV) оксида выражены ярче.
Применение
Сернистый газ используют для добывания кальций гідрогенсульфіту, который применяют при переработке древесины на целлюлозу. Сульфур(ИV) оксид необходимый для отбеливания текстильных изделий, уничтожение вредителей, чтобы сохранить овощи и фрукты от плесени и гнилостных микробов. В значительных количествах сернистый газ используют для добывания серной кислоты. Также его используют в текстильной промышленности для отбеливания тканей.
Сульфур(V) оксид
Сульфур(V) оксид (сульфур триоксид, серный ангидрид) SO3 - это высший оксид Серы.
Физические свойства и физиологическое действие
При стандартных условиях - это бесцветная летучая жидкость с резким запахом, которая состоит из циклических тримеров (SO3)3. Это токсичное вещество, которое поражает слизистые оболочки и дыхательные пути. При температуре 16,8 °С затвердевает и превращается в прозрачную кристаллическую массу. Отдельные молекулы в газообразном состоянии имеют форму плоского правильного треугольника. Все атомы расположены в одной плоскости. Валентные углы составляют 120°:
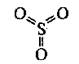
Добыча сульфур(VИ) оксида
Лабораторные способы:
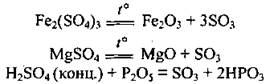
Промышленный способ (катализаторы - Pt, V2O5):
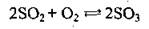
Химические свойства сульфур(VИ) оксида
1. Сульфур(V) оксид проявляет общие свойства кислотных оксидов: энергично:реагирует с водой, взаимодействует с основными и амфотерными оксидами, а также с гидроксидами, образуя кислые или средние соли:
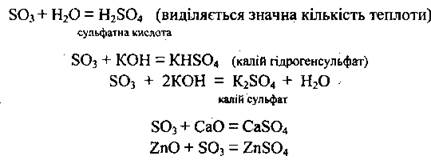
2. Сульфур(V) оксид растворяется в безводной сульфатной кислоте, образуя олеум. Обычно олеум содержит 18-20 % SO3 (иногда до 60 %).
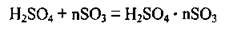
Олеум содержит и піросульфатні кислоты:
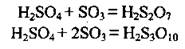
3. Сульфур(V) оксид проявляет сильные окислительные свойства, потому что Сульфур в этом соединении имеет максимальную степень окисления: